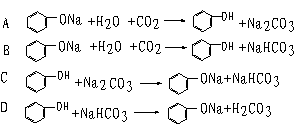|
烃的衍生物误点警示 湖北省巴东县第二高级中学 田宗学 烃的衍生物是中学有机化学的核心内容,考试中出现的频率也非常高。在复习时要抓住各类烃的衍生物的重要代表物的结构和官能团。官能团对物质的性质起决定性作用。因此需要我们在学习过程中去挖掘和积累,克服一些容易出现的误点。 一、苯酚的酸性 苯酚分子结构中含有—OH,显弱酸性,氢原子相对活泼,能与NaOH反应生成苯酚钠和水。不同于苯甲醇的结构,虽然苯甲醇也有—OH,但它属于醇类,不显酸性,不能与NaOH反应。 例1.已知酸性强弱顺序为H2CO3>
思路分析:可由较强的酸能与较弱的酸的盐反应生成较弱的酸和较强的酸的盐反应规律,以及题给的酸性强弱顺序来解答。根据碳酸能与苯酚钠反应,生成NaHCO3及苯酚,故A错,B对;根据苯酚与碳酸钠溶液反应生成碳酸氢钠,但不能与碳酸氢钠反应生成CO2和H2O,故C对,D错,所以B、C符合题意。 误区警示:不少同学对于本题误点是没有搞清楚苯酚钠与CO2、水的反应规律, 2 反应生成Na2CO3和苯酚;也会错误的认为苯酚与Na2CO3不反应,从而出现误选。苯酚显弱酸性,碳酸钠的碱性相对较强,两者不能共存,不论CO2是否过量,产物均为NaHCO3。 答案:B、C 二、有机物多官能团性质的判断 烃的衍生物的官能团不同,表现出的性质不同,而且具有同一官能团的物质,由于原子(或原子团)的影响,又表现出相异的性质。化学性质取决于物质结构,因此若结构中有多种官能团,则应具有每种官能团的性质。根据物质中的官能团和每种官能团对应的代表物的性质,来确定该陌生有机物的性质。同时培养他们对知识的归纳、迁移、分析推理能力。 例2:丁香油酚的结构简式为: 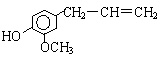 。从它的结构简式可推测它不可能有的化 。从它的结构简式可推测它不可能有的化学性质是 ( ) A.既可燃烧,也可使酸性KMnO4溶液褪色 B.可与NaHCO3溶液反应放出CO2气体 C.可与三氯化铁溶液发生显色反应 D.可与溴水发生反应 思路分析:由该物质的结构简式可知:丁香油酚是一种含多种官能团的复杂有机物。分子中含有C、H元素,一般来讲可以燃烧;含C=C双键,可发生与Br2的加成反应,也可被酸性KMnO4溶液氧化;苯环上连有—OH,属于酚类,可与强碱NaOH溶液反应,但不能与NaHCO3溶液反应放出CO2气体。分子中的三种官能团:C=C,—OH,C—O—C(醚键),都不能水解,故答案为B。 误点警示:有机化合物体现的是官能团的性质,但一个复杂的有机物含有多个官能团时,它应当拥有多类化合物的性质。目的是考查学生对多官能团有机物性质的认识能力。 答案:B 例3:阿斯匹林是一种古老常用的解热镇痛抗感冒药物。又称乙酰水杨酸,是苯环上连邻位一个乙酰基和一个碳的羧基。阿司匹林的结构简式为: 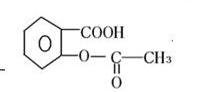 1mol阿司匹林与足量烧碱溶液共热,充分反应后消耗NaOH的物质的量是( )A.1mol B.2mol C.3mol D.4mol 思路分析:能直接和NaOH反应的有—COOH、酯基。先酯水解。“酯基”消耗1molNaOH。酯基水解之后 得到酚羟基和—COOH,水解后苯环上得到一个羟基,叫做“酚羟基”。酚羟基和—COOH均可与NaOH发 生反应。此时“酚羟基”和苯环上“羧基”都分别能消耗1molNaOH。 酯类物质水解之后得到的羧基可以消耗NaOH,得到的羟基,如果连在苯环上,同样可以消耗NaOH。所 以总共消耗 3mol NaOH。答案选 C 误点警示:同学们容易忽略酯基与NaOH的反应而误选A;还有可能忽略阿司匹林水解生成的酚羟基也能 与NaOH反应而消耗更多的NaOH,因此误选B。 答案:C 三、物质的除杂与分离方法 化学常用的物质的分离方法很多,一般有以下几种: 1.溶解过滤法:一种物质易溶于水,另一种物质难溶于水,可以将这两种物质的混合物溶于水,然 后过滤,就可以分离出这两种物质。 2.冷却热饱和溶液法:根据两种物质的在水中的溶解度有较大的差异。将这两种物质的混合物配制 成混合溶液,然后突然降低温度,溶解度较小的那种物质就结晶析出了,因此,就将这两种物质分 离出来了。 3.物质溶解特性法(萃取法):两种物质的混合物中,有一种物质不容于有机溶剂,而另一种物质 易溶于有机溶剂,且这两种物质都不和有机溶剂反应,可根据这种特性,先将其中的一种物质溶解 在这种有机溶剂中,产生分层的现象,然后分离出它们。 4.气体沉淀法:两种物质的混合物中,有一种物质能和其它的物质发生反应,产生沉淀或者是气体, 而另一种物质不反应,利用这种性质,将这两种物质分离出来。 例4.写出除去下列物质中的杂质(括号内),可选用的试剂和方法。
思路分析:在第一项中,学生易错填“浓溴水、过滤”,虽然浓溴水与苯酚生成三溴苯酚沉淀, 但因它仍易溶于苯中而不易分离,故只能采取加NaOH溶液,让其与苯酚反应生成可溶性的苯酚 钠溶液,然后采用“分液”操作进行分离。在第二项中,学生易错填NaOH溶液,因在NaOH溶液中 ,乙酸乙酯极易发生水解反应。还有一部分学生填“饱和Na2CO3溶液”时漏掉“饱和”二字而 失分。第四项中,因对加入“CaO”试剂的作用不清楚,而采取直接“蒸馏”的方法,实际上 乙醇和水都易挥发,加入CaO的目的是起到“固定”水的作用。 例5.欲从苯酚的乙醇溶液中回收苯酚,有下列操作:①蒸馏 ②过滤 ③静置分液 ④加入 足量的金属钠 ⑤通入过量的二氧化碳 ⑥加入足量的NaOH溶液 ⑦加入足量的FeCl3溶液 ⑧加入乙酸与浓硫酸混合液加热。合理的步骤顺序是( ) A.④⑤③ B.⑥①⑤③ C.⑧① D.⑧②⑤③ 思路分析:有机物形成的混合溶液要想分离,一般采用蒸馏的方法。但是针对本题,苯酚的 乙醇溶液,常规方法蒸馏,苯酚易被氧化,无法回收。所以只好采用转变晶型,先进行步骤⑥, 使苯酚变为苯酚钠(离子晶体),沸点高,易溶于水。然后进行①蒸馏,乙醇馏出。留下苯 酚钠的水溶液。接着向其中通入过量的CO2(⑤),苯酚钠又变回苯酚,不易溶于水,两者静 置会分层,分液即可分离,回收了苯酚。选B项。许多学生易错选A。若先向溶液中加Na,苯 酚反应生成苯酚钠,乙醇反应生成乙醇钠,再进行步骤⑤。学生试想: 中无水,自然也就不能进行上述反应。故排除A项。C、D项中均有步骤⑧,加入了新的杂质, 在后续步骤中无法分离,故排除。 答案:B (责任编辑:admin) |