|
《化学能与热能》同步测试 贵州省遵义市第二中学 周厚彬 1.下列说法中正确的是( ) A.物质发生反应时放出的热量来源于对反应的加热 B.化学反应除了生成新物质外,还发生能量变化,且总表现为吸热 C.化学反应过程中有时吸热,有时放热 D.化学反应总是放出热量 考查目的:考查化学反应过程中的能量变化,有吸热和放热过程。 答案:C 解析:化学反应中总是伴有能量的变化,且能量通常以热的形式表现出来,有吸热和放热过程。 2.已知断裂1mol共价键所需要吸收的能量分别为H—H键:436 kJ;I—I键:153 kJ;H—I键:229 kJ。下列对反应H2(g)+I2(g)=2HI(g)的判断中,错误的是( ) A.该反应是放出能量的反应 B.该反应是吸收能量的反应 C.该反应是氧化还原反应 D.I2与H2具有的总能量大于生成的HI具有的总能量 考查目的:考查氧化还原反应的判断,根据键能计算判断吸热反应和放热反应。 答案:B 解析:依题意,断裂1mol H—H键和1mol I—I键吸收的总能量为436 kJ+153 kJ=589 kJ,生成2mol H—I键放出的能量为299 kJ×2=598 kJ,因598 kJ>589 kJ,所以H2与I2反应生成HI的反应是放出能量的反应;根据反应式可知该反应是氧化还原反应。 3.一种化学冰袋中含有Na2SO4·10H2O和NH4NO3,使用时将它们混合用手搓揉就可制冷,且制冷效果能维持一段时间。以下关于其制冷原因的推测错误的是( ) A.Na2SO4·10H2O脱水是吸热过程 B.较长时间制冷是由于Na2SO4·10H2O脱水是较慢的过程 C.铵盐在该条件下发生的复分解反应是吸热反应 D.NH4NO3溶于水会吸收热量 考查目的:考查吸热反应,意在考查学生依据题干分析推理能力。 答案:C 解析:Na2SO4·10H2O失水属于分解反应,吸热反应;NH4NO3吸收水并溶解于水中,是一个吸热的物理变化过程,整个过程中只是Na2SO4·10H2O的分解反应和NH4NO3溶于水的过程,而并没有发生复分解反应,C项错误。 4.化学反应A2+B2 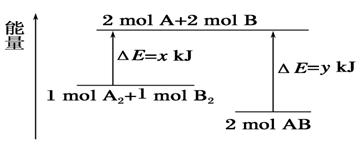 A.该反应是吸热反应 B.断裂1mol A—A键和1mol B—B键能放出x kJ的能量 C.断裂2mol A—B键需要吸收y kJ的能量 D.2mol AB的总能量高于1 mol A2和1mol B2的总能量 考查目的:考查化学反应中的热效应,意在考查学生读图能力。 答案:C 解析:由图像知,1mol A2和1mol B2的总能量高于2mol AB的能量,所以该反应放热。 5.下列反应既是氧化还原反应,又是吸热反应的是( ) A.铝片与稀H2SO4反应 B.Ba(OH)2·8H2O与NH4Cl反应 C.灼热的炭与CO2反应 D.甲烷在O2中的燃烧反应 考查目的:考查氧化还原反应和吸热反应的判断。 答案:C 解析:A、D是放热反应,B、C是吸热反应,但Ba(OH)2·8H2O+2NH4Cl===BaCl2+2NH3·H2O+8H2O是非氧化还原反应,C+CO22CO是氧化还原反应,故选C。 6.(体验高考)下列说法正确的是( ) A.需要加热的化学反应都是吸热反应 B.中和反应都是放热反应 C.原电池是将电能转化为化学能的一种装置 D.水力发电是将化学能转化为电能的过程 考查目的:考查热效应、原电池等基本概念。 答案:B 解析:需要加热的化学反应也可能是放热反应,如可燃物的燃烧,A选项错误;原电池是将化学能转化为电能的装置,故C选项错误;水力发电是将机械能转化为电能的过程,故D选项错误。正确选项为B。 7.(体验高考)下列有关能量转换的说法正确的是 ( ) A.煤燃烧是化学能转化为热能的过程 B.化石燃料和植物燃料燃烧时放出的能量均来源于太阳能 C.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程[来源:学&科&网Z D.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程 考查目的:考查化学反应中的能量转化关系。 答案:AB 解析:葡萄糖氧化放出热量,化学能转化为热能,C错;选项D应该太阳能转化为化学能,D错。 8.氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1mol 氢气中的化学键消耗的能量为Q1kJ,破坏1mol氯气中的化学键消耗的能量为Q2kJ,形成1mol氯化氢中的化学键释放的能量为Q3kJ。下列关系式中,正确的是( ) A.Q1+Q2>Q3 B.Q1+Q2>2Q3 C.Q1+Q2<Q3 D.Q1+Q2<2Q3 考查目的:考查化学反应中的热效应,依据反应类型判断能量大小。 答案:D 解析:H2+Cl2 9.已知H++OH-===H2O生成1mol H2O放出热量57.3 kJ,下列反应中符合该特点的是( ) A.1mol稀H2SO4与足量NaOH溶液反应 B.稀盐酸与氨水反应生成1mol H2O C.稀盐酸与稀Ba(OH)2溶液反应生成1mol水 D.稀NaOH与95%浓硫酸反应生成1mol水 考查目的:考查中和热。 答案:C 解析:A放出热量应为2mol×57.3 kJ/mol;B放出热量(即中和热)应略小于57.3 kJ,因弱酸、弱碱在水中电离要吸收一部分热量,故多数强酸与弱碱,弱酸与强碱的中和反应热值小于57.3 kJ。酸与碱的浓度不能太大,否则中和热数值会偏大,故D错。 10.(体验高考)白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ·mol—1、P—O b kJ·mol—1、P=O c kJ·mol—1、O=O d kJ·mol—1。 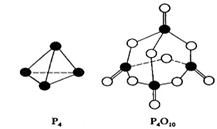 根据图示的分子结构和有关数据估算该反应的△H,其中正确的是 ( ) A.(6a+5d-4c-12b)kJ·mol—1 B.(4c+12b-6a-5d)kJ·mol—1 C.(4c+12b-4a-5d)kJ·mol—1 D.(4a+5d-4c-12b)kJ·mol—1 考查目的:考查化学反应中的热效应,△H的计算,意在考查考生读图分析能力。 答案:A 解析:由图可以看出:P4中有6mol的P-P,5mol的O2中含有5molO=O,1mol的P4O10中含有4mol的P=O,12mol的P-O,所以△H=(6a+5d-4c-12b)kJ·mol-1。 二、非选择题 11.(体验高考)下表中的数据是破坏1mol物质中的化学键所消耗的能量:
根据上述数据回答下列问题: (1)下列物质本身具有的能量最低的是( ) A.H2 B.Cl2 C.Br2 D.I2 (2)下列氢化物中最稳定的是( ) A.HCl B.HBr C.HI (3)X2+H2===2HX(X代表Cl、Br、I)的反应是吸热反应还是放热反应?________。 (4)相同条件下,X2(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是________。 考查目的:考查化学反应中的热效应,吸热反应和放热反应的判断、焓变的计算、物质稳定性的判断知识,意在考查考生依据表格分析计算的能力。 答案:(1)A (2)A (3)放热反应 (4)Cl2 解析:(1)、(2)破坏1mol物质中的化学键所消耗的能量越大,则物质越稳定,所具有的能量越低。(3)、(4)以氯元素为例计算断开1mol Cl—Cl键和H—H键需吸收能量: 243 kJ+436 kJ=679 kJ,而形成2mol HCl放出的能量为2×432 kJ=864 KJ,所以在Cl2+H2===2HCl反应中放出864 kJ-679 kJ=185 kJ的热量,同理可计算在Br2+H2===2HBr、I2+H2===2HI反应中分别放出103 kJ、9 kJ的热量。 12.为了探究化学能与热能的转化,某实验小组设计了如下三套实验装置: 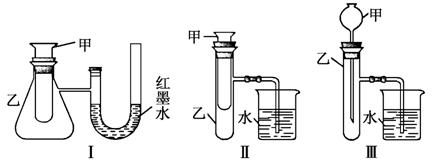 (1)上述3个装置中,不能证明”铜与浓硝酸反应是吸热反应还是放热反应”的是________。 (2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U形管中可观察到的现象是________________,说明该反应属于________(填“吸热”或“放热”)反应。 (3)为探究固体M溶于水的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。①若M为钠,则实验过程中烧杯中可观察到的现象是________;②若观察到烧杯里产生气泡,则说明M溶于水________(填“一定是放热反应”“一定是吸热反应”或“可能是放热反应”),理由是________________________________________; ③若观察到烧杯里的玻璃管内形成一段水柱,则M可能是__________________。 (4)至少有两种实验方法能证明超氧化钾与水的反应(4KO2+2H2O===4KOH+3O2↑)是放热反应还是吸热反应。方法①:选择上述装置________(填“Ⅰ”“Ⅱ”或“Ⅲ”)进行实验;方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是________反应。 考查目的:考查化学反应中热效应的实验,意在考查学生实验综合分析能力,特别是实验的评价和根据实验现象推理的能力。 答案:(1)Ⅲ (2)左端液柱降低,右端液柱升高 放热 (3)①产生气泡,反应完毕后,冷却至室温,烧杯里的导管内形成一段液柱 ②可能是放热反应 某些物质(如浓硫酸)溶于水放热,但不是放热反应 ③硝酸铵(或其他合理答案) (4)Ⅰ(或Ⅱ) 放热 解析:(1)装置Ⅰ可通过U形管中红墨水液面的变化判断铜与浓硝酸的反应是放热还是吸热;装置Ⅱ可通过烧杯中是否产生气泡判断铜与浓硝酸的反应放热还是吸热;装置Ⅲ只是一个铜与浓硝酸反应并将生成的气体用水吸收的装置,不能证明该反应是放热反应还是吸热反应。 (2)氢氧化钡与硫酸反应属于中和反应,中和反应都是放热反应。(3)浓硫酸、硝酸铵溶于水有热效应,但不属于化学反应,故不是放热或吸热反应。 (责任编辑:admin) |
