|
《生活中两种常见的有机物》同步测试(第1课时) 贵州省遵义市第二中学 周厚彬 一、选择题 1.(体验高考)全国首例“酒驾入刑”由河南省舞钢市人民法院判决,以“危险驾驶罪”判处被告人侯××拘役4个月,并处罚金2000元。目前,交警对驾驶员是否酒后驾驶的一种测定原理是:橙色的酸性K2Cr2O7遇呼出的乙醇蒸气迅速生成蓝绿色的Cr3+。下列关于乙醇的性质中,与此测定原理有关的是( )  图 K27-1 ①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇与水以任意比互溶 ⑤乙醇可燃烧 ⑥乙醇是烃的含氧化合物 A.②⑤ B.②④⑥ C.①③ D.①③⑥ 考查目的:考查乙醇性质 答案:C 解析:乙醇沸点低,易挥发,故易被检测。酸性K2Cr2O7具有强氧化性,可以氧化乙醇,自身生成Cr3+。 2.能证明乙醇分子中有一个羟基的事实是( ) A.乙醇完全燃烧生成CO2和H2O B.0.1mol乙醇与足量的钠反应生成0.05mol氢气 C.乙醇能溶于水 D.乙醇能脱水 考查目的:考查乙醇的化学性质和结构。 答案:B 解析:乙醇与生成的氢气的物质的量之比为0.1:0.05=2:1,说明乙醇分子中有一个活泼的氢原子可被金属钠取代(置换),即乙醇分子中有一个羟基。 3.据美国权威机构麦肯锡分析,随着低碳经济概念的提出与完善,纤维素乙醇产业对中国的潜在贡献巨大。乙醇是一种比较理想的再生能源,目前新兴起的车用乙醇汽油就是掺入一定比例乙醇的汽油。下列说法正确的是( ) A.在相同状况下,同体积的乙醇气体和乙烯气体都完全燃烧,耗氧量不同 B.在相同状况下,同体积的乙醇气体和乙烯气体都完全燃烧,产物相同,产物的量也相同 C.用乙醇作燃料不会导致“温室效应” D.用乙醇作燃料不会导致酸雨 考查目的:考查化学与生活,意在考查乙醇和乙烯的性质。 答案:D 解析:乙醇的分子式为C2H6O,可以写成C2H4·H2O,相同状况,同体积的乙醇气体和乙烯气体完全燃烧时,耗氧量相同、产物相同,乙醇燃烧后产生二氧化碳和水,不会产生酸雨。 4.C2H5OH的官能团是—OH,含有—OH的物质具有与乙醇类似的化学性质,在Cu或Ag催化下,下列物质不能与O2发生氧化反应的是( ) 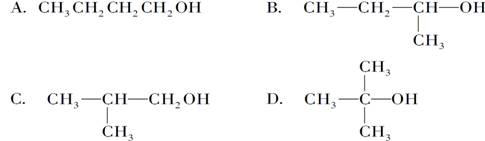 考查目的:考查乙醇的催化氧化。 答案:D 解析:由乙醇的催化氧化原理 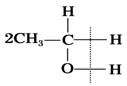 +O2Cu或Ag△2CH3—CHO+2H2O知,只有连有—OH的碳原子上有氢原子的醇才能发生催化氧化,故选D。 +O2Cu或Ag△2CH3—CHO+2H2O知,只有连有—OH的碳原子上有氢原子的醇才能发生催化氧化,故选D。5.下列物质,都能与Na反应放出H2,其产生H2的速率排列顺序正确的是( ) ①C2H5OH ②H2CO3溶液 ③H2O A.①>②>③ B.②>①>③ C.③>①>② D.②>③>① 考查目的:考查元素化合物的性质。 答案:D 解析:Na与H2O反应比与C2H5OH反应剧烈,故反应速率③>①,可排除A、B两项。H2CO3溶液中不仅含有H2O,而且含有H2CO3,H2CO3电离出H+使溶液呈酸性,Na与H2CO3反应比与H2O反应剧烈得多,故可知反应速率排序为②>③>①。 6.按下图装置,持续通入X气体,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体是( ) 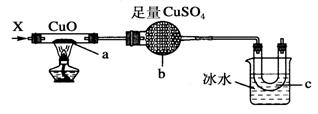 A.H2 B.CO和H2 C.NH3 D.CH3CH2OH(气) 考查目的:考查化学实验和乙醇的化学性质。 答案:D 解析:根据a处有红色物质生成,说明该气体被CuO还原;b处变蓝,说明发生氧化反应过程中有水生成;c处得到液体,说明该反应除生成水外,还生成了易液化的物质,符合该条件的只有乙醇蒸气。 7.丙烯醇(CH2===CH—CH2OH)可发生的化学反应有( ) ①加成 ②氧化 ③燃烧 ④加聚 ⑤取代 A.只有①②③ B.只有①②③④ C.①②③④⑤ D.只有①③④ 考查目的:考查有机物官能团的性质。 答案:C 解析:丙烯醇含有两种官能团:C===C和—OH,所以它应具有烯和醇的化学性质。 8.一定量的乙醇在氧气不足的情况下燃烧,得CO、CO2和水的总质量为27.6g,若其中水的质量为10.8g,则CO的质量为( ) A.1.4g B.2.2g C.4.4g D.在2.2g与4.4g之间 考查目的:考查乙醇的可燃性和混合物质量的计算,意在考查元素的质量守恒的应用。 答案:A 解析:运用C2H5OH中C与H原子个数列方程组解答。此题要利用元素的质量守恒。先利用乙醇与水中氢元素质量守恒,由水的质量计算出乙醇的物质的量:×=0.2mol。再由乙醇中碳与CO、CO2中所含碳元素守恒,列式计算。 设CO的物质的量为x,CO2的物质的量为y,则: 解得 则m(CO)=0.05mol×28g·mol-1=1.4g。 9.(体验高考)乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法不正确的是( ) 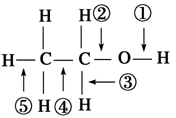 A.和金属钠反应时键①断裂 B.在铜催化共热下与O2反应时断裂①和③ C.在铜催化共热下与O2反应时断裂①和⑤ D.在空气中完全燃烧时断裂①②③④⑤ 考查目的:考查乙醇的分子结构和化学性质。 答案:C 解析:乙醇与钠反应生成乙醇钠,是羟基中的O—H键断裂,A正确;乙醇催化氧化成乙醛时,断裂①和③化学键,B正确,C错误;乙醇完全燃烧时,化学键①②③④⑤全部断裂。 10.酒精灯的火焰分为三层,由外到内依次为外焰、内焰、焰心,若把一根洁净的铜丝,由外焰逐渐深入到内焰,能观察到的现象是( ) A.始终是红色 B.由红色变为黑色 C.在外焰变为黑色,到内焰变为红色 D.在外焰是红色,到内焰变为黑色 考查目的:考查乙醇的催化氧化和观察分析的能力。 答案:C 解析:铜丝在酒精灯的外焰被氧化而变为黑色,渐渐深入到内焰时,由于内焰温度低,一些没有燃烧的乙醇蒸气将氧化铜还原而变为红色。 二、非选择题 11.(体验高考)生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇和乙酸是比较常见的有机物。 (1)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为____________________。(不用写反应条件),原子利用率是________。 (2)乙醇能够发生氧化反应。 乙醇在铜作催化剂的条件下可被氧气氧化为乙醛,反应的化学方程_________________。 (3)下列关于乙醇的说法正确的是________(选填字母)。 A.乙醇不能和酸性高锰酸钾溶液发生氧化还原反应 B.交警用橙色的酸性重铬酸钾溶液检查司机是否酒后驾车 C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了 (4)做菜时既加醋又加酒可以增加菜的香味,其原因是生成了酯类物质,写出该反应的化学方程式_________________________________________,该反应的反应类型________。 (5)当乙酸分子中的O都是18O时,乙醇分子中的O都是16O时,二者在一定条件下反应,生成物中水的相对分子质量为________。 考查目的:考查乙醇的制取、性质,意在考查考生化学用语、有机反应方程式的正确书写及反应类型的判断。 答案:(1)CH2===CH2+H2O―→CH3CH2OH 100%;(2)2CH3CH2OH+O2Cu△2CH3CHO+2H2O;(3)B、C(4)CH3COOH+CH3CH2OH (5)20 解析:(3)醋的主要成分为CH3COOH,酒的主要成分为CH3CH2OH,二者可以发生酯化反应生成CH3COOCH2CH3。 (5)乙酸与乙醇反应的化学方程式为: C H3C18O18OH+H16O—C2H5 12.某实验小组用下列装置进行乙醇催化氧化的实验。  (1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式:________,_____________________。在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇的氧化反应是________反应。 (2)甲和乙两个水浴的作用不相同。甲的作用是______________________;乙的作用是_______________________________________。 (3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是________。集气瓶中收集到的气体的主要成分是________。 (4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有________。要除去该物质,可先在混合液中加入_ _(填写字母)。 a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳 然后,再通过________(填实验操作名称)即可除去。 考查目的:考查有机化学实验,意在考查乙醇的催化氧化、结构简式、有机化学方程式的书写和装置的用途、除杂等知识。 答案:(1)2Cu+O22CuO CH3CH2OH+CuOCH3CHO+Cu+H2O 放热 (2)加热 冷却 (3)乙醛、乙醇、水 氮气 (4)乙酸 c 蒸馏 解析:该实验目的是:乙醇的催化氧化。实验原理:2Cu+O22CuO,CH3CH2OH+CuOCH3CHO+H2O+Cu。 实验流程:甲中的水为热水,其作用是将无水乙醇加热成乙醇蒸气,与空气一起进入玻璃管中,在铜网的作用下进行反应后,从玻璃管中出来的物质有:未反应的乙醇蒸气及少量O2、水蒸气、乙醛蒸气和大量的N2,它们一起进入乙中,乙中的水为冷水,其作用是将乙醇蒸气、水蒸气、乙醛蒸气进行冷却变为液体,不能冷却的少量O2和大量的N2进入到集气瓶中。(4)由题意知,该物质呈酸性,说明该物质为乙酸。若要除去乙醇、水、乙醛中的乙酸,可先在混合液中加入NaHCO3溶液,发生CH3COOH+NaHCO3===CH3COONa+H2O+CO2↑反应,使CH3COOH转化为CH3COONa,再通过蒸馏即可除去。 (责任编辑:admin) |
