|
氨 喷泉习题 1.下列气体中,不会造成空气污染的是( ) A.N2 B.NO C.NO2 D.CO 2.下列气体中,不能用排空气法收集的是( ) A.CO2 B.H2 C.NO2 D.NO 3.通常状况下能共存,且能用浓硫酸干燥的一组气体是( ) A.H2、O2、N2 B.O2、NO、NO2 C.H2、N2、NH3 D.NH3、HCl、NO2 4.试管中盛有少量白色固体,可能是铵盐,检验的方法是( ) A.加水,将湿润的红色石蕊试纸放在试管口 B.加氢氧化钠溶液,加热,将湿润的红色石蕊试纸靠近试管口 C.加氢氧化钠溶液,加热,滴入酚酞试剂 D.加氢氧化钠溶液,加热,滴入紫色石蕊试剂 5.能把Na2SO4、NH4NO3、KCl和(NH4)2SO4四瓶无色溶液加以区别(必要时可加热)的一种试剂( ) A.BaCl2 B.Ba(NO3)2 C.Ba(OH)2 D.NaOH 6.氮气的性质是( ) A.只有氧化性 B.只有还原性 C.既有氧化性又有还原性 D.既没有氧化性又没有还原性 7.下列气体易液化,遇挥发性酸时冒白烟,而且适宜作致冷剂的是( ) A.N2 B.NH3 C.NO D.NO2 8.氨水显弱碱性的主要原因是( ) A.通常状况下,氨的溶解度不大 B.氨水中的NH3·H2O电离出少量OH- C.溶于水的氨分子只有少量电离 D.氨本身的碱性弱 9.两个体积相同的容器,一个盛有一氧化氮,另一个盛有氮气和氧气,在同温同压下两容器内的气体一定具有相同的( ) A.原子总数 B.质子总数 C.分子总数 D.质量 10.在右下图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧瓶中的液体b呈喷泉状喷出,最后几乎充满烧瓶。则a和b分别是( )
11.在体积为V升的密闭容器中通入a摩NO和b摩O2,反应后容器内氮原子数和氧原子数之比为( )   12.已知25%氨水的密度为0.91g.cm-3,5%氨水的密度为0.98g.cm-3,若将上述两溶液等体积混合,所得氨水溶液的质量分数是( ) A. 等于15% B.大于15% C.小于15% D.无法估算 13.在1L浓度为1mol/L的氨水中( ) A.含有1molNH3分子 B.含有NH3和NH4+之和为1mol C.含NH3·H2O1mol D.含NH3、NH3·H2O、NH4+之和为1mol 14.某无色混合气体,依次通过浓硫酸和过氧化钠,气体体积不断减少,颜色变深,则混合气体组成是( ) A.H2O(g)、NO和N2 B.NO2、CO2和H2O(g) C.O2、HCl和CO D.NH3、NO和CO2 15.同温同压下,两个等体积的干燥烧瓶中分别充满①NH3 ②NO2,进行喷泉实验,;经充分反应后,瓶内溶液的物质的量浓度为( ) 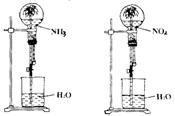 A.①>② B.①<② C.①=② D.不能确定 16.X、Y、Z三种气体都是大气污染物,在工业上通常都用碱液吸收。已知X是化石燃料燃烧的产物之一,是造成酸雨的主要物质;Y是一种单质,其水溶液具有漂白作用,Z是硝酸工业和汽车尾气中的有害物质之一,易溶于水。请写出下列有关反应的化学方程式。 ⑴X在一定条件下与氧气反应; ⑵Y与消石灰反应; ⑶Z溶于水。 17.实验室中要测定某无色气体的成分,已知此气体可能由CO2、NH3、NO2、N2、NO中的一种或几种混合而成。对此无色气体进行以下实验: ①先通过盛有浓硫酸的洗气瓶,发现气体减少一部分体积; ②继续通过装有Na2O2固体的干燥管,发现从干燥管出来的气体颜色呈红棕色; ③再继续将气体通入盛满水倒立于水槽中的试管内,最后气体完全被吸收,试管内仍为一满试管液体。由此可判断: (1)原气体中一定含有________ ,一定不含有_________________ 。 (2)写出②中发生反应的化学方程式:______________________ ________________________________________________________________________ 。 (3)由最终结果可知原气体中________ 和________ 的体积比为________ 。 18.将盛有12 mLNO2和O2的混合气体的量筒倒立于水槽中,充分反应后,还剩余2 mL无色气体,则原混合气体中O2的体积是多少? (责任编辑:admin) |
