|
(6)SiO2 :原子晶体,空间网状结构,Si原子构成正四面体,O原子位于Si-Si键中间。(SiO2晶体中不存在SiO2分子,只是由于Si原子和O原子个数比为1∶2,才得出二氧化硅的化学式为SiO2) 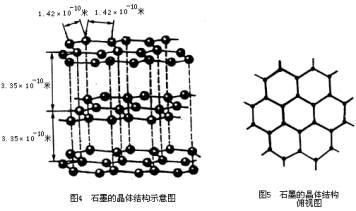 石墨的晶体结构示意图及石墨的晶体结构俯视图 3.离子晶体化学式的确定 确定离子晶体的化学式实际上是确定晶体中粒子个数比。其方法如下: (1)处于顶点的粒子,同时为8个晶胞所共有,每个粒子有1/8属于该晶胞。 (2)处于棱上的粒子同时为4个晶胞共有,每个粒子有1/4属于该晶胞。 (3)处于面心上的粒子,同时为2个晶胞共有,每个粒子有1/2属于该晶胞。 (4)处于晶胞体心的粒子,则完全属于该晶胞。 4.根据物质的物理性质判断晶体的类型 (1)在常温下呈气态或液态的物质,其晶体应属于分子晶体(Hg除外),如H2O、H2等。对于稀有气体,虽然构成物质的微粒为原子,但应看作单原子分子,因为微粒间的相互作用力是范德华力,而非共价键。 (2)在熔融状态下能导电的晶体(化合物)是离子晶体。如:NaCl熔融后电离出Na+和Cl-,能自由移动,所以能导电。 (3)有较高的熔、沸点,硬度大,并且难溶于水的物质大多为原子晶体,如晶体硅、二氧化硅、金刚石等。 (4)易升华的物质大多为分子晶体。 三、分子间作用力和氢键 1.分子间作用力 分子间作用力又叫范德华力,是分子与分子之间微弱的相互作用,它不属于化学键范畴。分子间作用力广泛存在于分子与分子之间,由于相互作用很弱,因此只有分子与分子充分接近时,分子间才有作用力。 2.氢键 氢键是在分子间形成的,该分子中必须含有氢原子,且另一种原子吸引电子的能力很强(具体有F、O、N三种元素),只有这样才能形成氢键。常见的能形成氢键的分子主要有HF、H2O、NH3等。 氢键的实质也是静电作用,氢键的强度比分子间作用力稍强,但比化学键弱的多,它仍不属于化学键范畴。 氢键对物质熔、沸点的影响结果是使物质的熔点和沸点均升高。例如H2O和H2S的组成与结构相似,相对分子质量H2S>H2O,若仅以分子间作用力论,H2S的熔、沸点应大于H2O,可实际上H2O在常温状态下是液态,而H2S在通常状态下是气态,说明H2O的熔、沸点比H2S高,原因就是H2O分子中存在H…O键。 四、物质的熔沸点比较及规律 (1)不同类型的晶体,一般来讲,熔沸点按原子晶体>离子晶体>分子晶体。 (2)由共价键形成的原子晶体中,原子半径越小的,键长越短,键能越大,晶体的熔、沸点越高。如熔点:金刚石>石英>碳化硅>晶体硅。 (3)离子晶体比较离子键的强弱。一般地说,阴、阳离子的电荷数越多,离子半径越小,则离子间的作用就越强,其离子晶体的熔沸点就越高,如熔点:MgO>MgCl2>NaCl>CsCl。 (4)分子晶体:组成和结构相似的物质,相对分子质量越大,熔沸点越高;如Cl2<Br2<I2。组成和结构不相似的物质,分子极性越大,其熔沸点就越高,如熔、沸点:CO>N2。 [例题分析] 例1.下面的叙述正确的是 A、离子化合物中可能含有共价键 B、分子晶体中不会有离子键 C、分子晶体中的分子内一定有共价键 D、原子晶体中一定有非极性共价键 [分析与解答] 若离子化合物中某种离子由两种或两种以上元素组成。如NH4+、OH-、SO42-等。则其离子内部有共价键。分子晶体的构成微粒是分子,分子间只有分子间作用力,分子内除稀有气体外,都只有共价键,故(A)、(B)正确。(C)未提到稀有气体分子是单原子分子,无任何化学键。由两种原子形成的原子晶体SiO2等,其原子间以极性键结合,无非极性键。故正确答案为(A)、(B)。 例2.下列各组物质的晶体中,化学键类型相同,晶体类型也相同的是 A、SO2和SiO2 B、CO2和H2O C、NaCl和HCl D、CCl4和KCl [分析与解答] A、SO2和SiO2的化学键相同,都是极性共价键,但晶体类型不同,SO2是分子晶体,SiO2是原子晶体; B、CO2和H2O的化学键都是共价键,且都属于分子晶体; C中的NaCl和HCl化学键类型不同,NaCl为离子键,HCl为极性共价键,且晶体类型也不同,NaCl为离子晶体,HCl为分子晶体; D中CCl4和KCl的化学键不同,CCl4是极性共价键,KCl中是离子键且晶体类型也不同,CCl4为分子晶体,KCl为离子晶体。 故正确答案为选项B。 例3.(1)中学教材上图示了NaCl晶体结构,它向三维空间延伸得到完美晶体。NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-的核间距离为a×10-8cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7g·mol-1)。 (2)天然的和绝大部分人工制备的晶体都存在各种缺陷。例如在某种NiO晶体中就存在如图7所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代。其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。某氧化镍品组成为Ni0.97O,试计算该晶体中Ni3+与Ni2+的离子数之比。 (责任编辑:admin) |
