|
自然界中的固体可以分为两种存在形式:晶体和非晶体。晶体是经过结晶过程而形成的具有规则的几何外形的固体。晶体中原子或分子在空间按一定规律周期性重复的排列,从而使晶体内部各个部分的宏观性质是相同的,而且具有固定的熔点和规则的几何外形。为了让大家更好的学习高中化学晶体的结构与性质知识点,高中学习网给大家整理了高中化学晶体的结构与性质知识点及相关例题讲解,希望对大家学习有帮助! 一、晶体 固体可以分为两种存在形式:晶体和非晶体。 晶体的分布非常广泛,自然界的固体物质中,绝大多数是晶体。气体、液体和非晶体在一定条件下也可转变为晶体。 晶体是经过结晶过程而形成的具有规则的几何外形的固体。晶体中原子或分子在空间按一定规律周期性重复的排列,从而使晶体内部各个部分的宏观性质是相同的,而且具有固定的熔点和规则的几何外形。 二、晶体结构 1.几种晶体的结构、性质比较
2.几种典型的晶体结构: (1)NaCl晶体(如图1):每个Na+周围有6个Cl-,每个Cl-周围有6个Na+,离子个数比为1:1。 (2)CsCl晶体(如图2):每个Cl-周围有8个Cs+,每个Cs+周围有8个Cl-;距离Cs+最近的且距离相等的Cs+有6个,距离每个Cl-最近的且距离相等的Cl-也有6个,Cs+和Cl-的离子个数比为1:1。 (3)金刚石(如图3):每个碳原子都被相邻的四个碳原子包围,以共价键结合成为正四面体结构并向空间发展,键角都是109º28',最小的碳环上有六个碳原子。 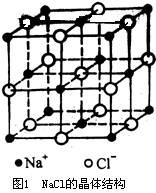 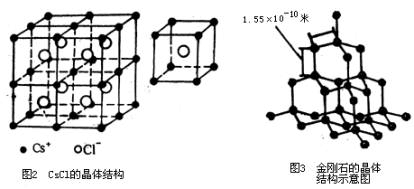 NaCl、CaCl以及金刚石的晶体结构示意图 (4)石墨(如图4、5):层状结构,每一层内,碳原子以正六边形排列成平面的网状结构,每个正六边形平均拥有两个碳原子。片层间存在范德华力,是混合型晶体。熔点比金刚石高。 (5)干冰(如图6):分子晶体,每个CO2分子周围紧邻其他12个CO2分子。 (责任编辑:admin) |
||||||||||||||||||||||||||||||||||||||||||||||||||
