|
寒假并不是休息的时候,而是2018年高考二轮复习的开始。这个阶段,考生已经有了一轮复习知识点的积累,所以重点就要放在能力提升。小编整理了2018高考化学二轮复习知识点专题,物质的提纯和分离、气体制备总结如下: 一、物质的提纯和分离(无机) (一)对混合物分离、提纯的基本要求:原理正确,操作简便,少用试剂,量不减少(或减少很少),保护环境。 (二)混合物分离、提纯常用的方法:按实验操作方法分类,将有关常用方法及其适应对象列表如下: 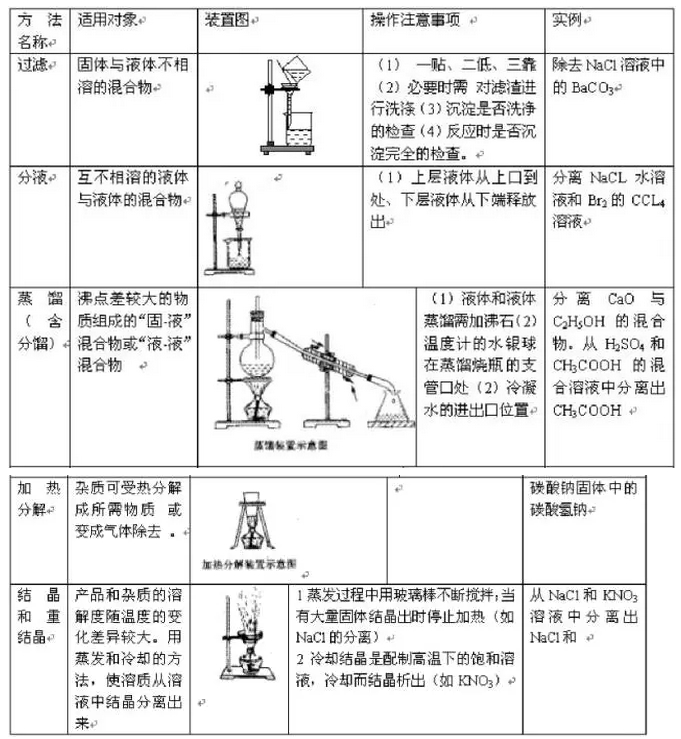 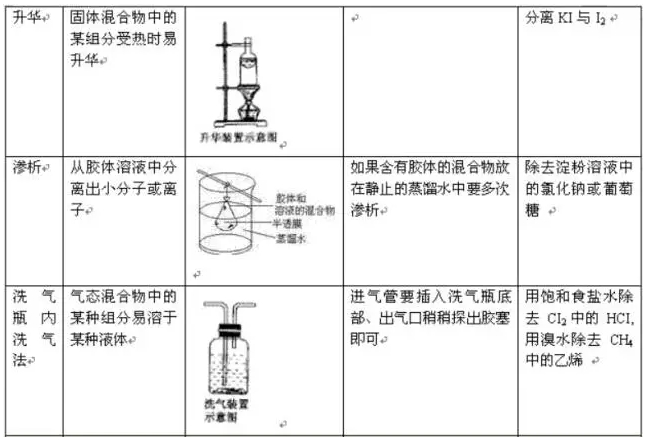 其它如: 加酸(某液体)转化法:溶液中的杂质遇酸转化为溶液中的主要成分或气体,如加硝酸除去硝酸钾溶液中的碳酸钾;通过量CO2除去NaHCO3溶液中的Na2CO3。 吸附法:混合物中的某种组分易被某种吸附剂吸附,如用木炭使蔗糖溶液脱去有机色素。 加氧化剂或还原剂转化法:溶液中的杂质易被氧化或还原为所需成分,如通氯气除去FeCl3溶液中的FeCl2,加铁除去FeCl2中的FeCl3。 常见物质除杂方法: 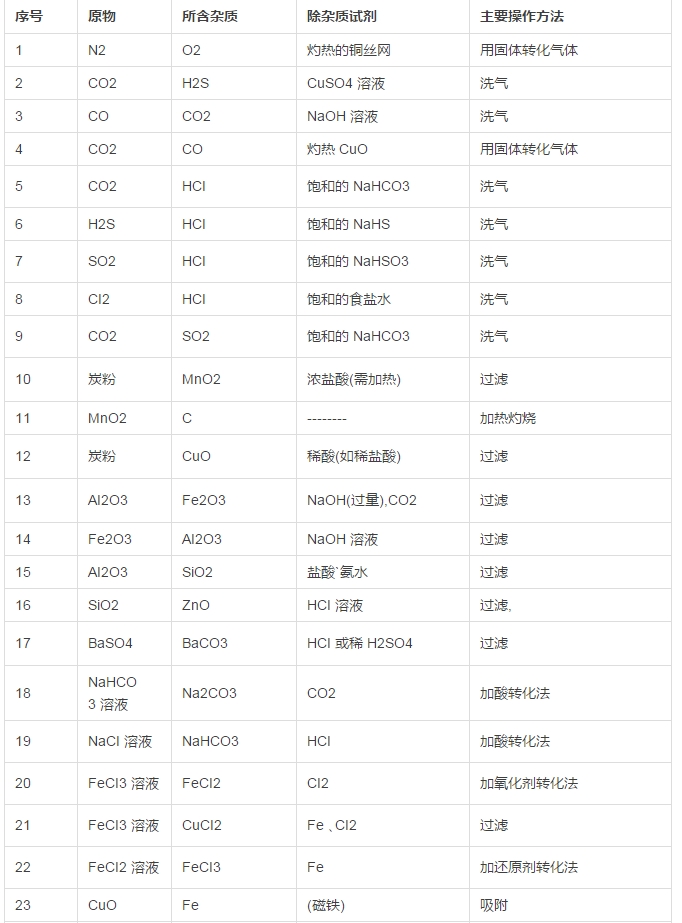  二、气体的制备 (一)气体实验装置的设计 1、装置顺序:制气装置→净化装置→反应或收集装置→除尾气装置 2、安装顺序:由下向上,由左向右 3、操作顺序:装配仪器→检验气密性→加入药品→进行实验 (二)气体发生装置的类型 1、设计原则:根据反应原理、反应物状态和反应所需条件等因素来选择反应装置。 2、装置基本类型: 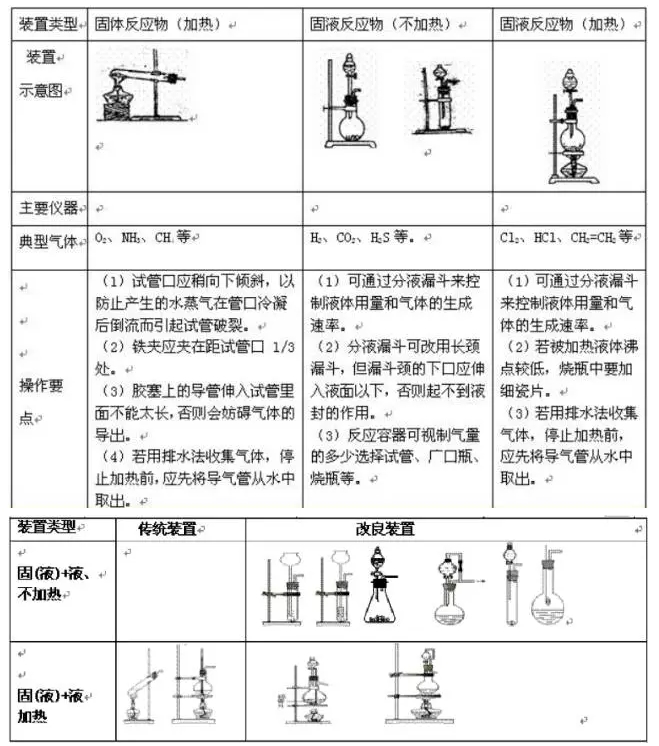 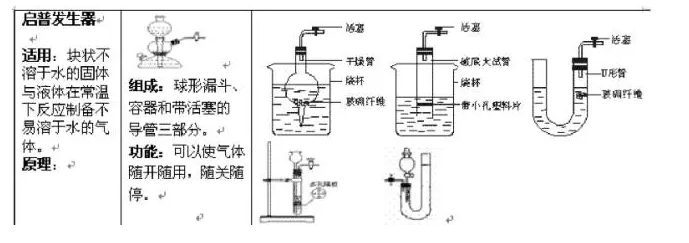 3、装置气密性的检验 把导管一端浸入水中,用双手捂住烧瓶或试管,借手的热量使容器内的空气膨胀(或用酒精灯加热),容器内的空气则从导管口形成气泡冒出,把手(酒精灯)拿开,过一会,水沿导管上升,形成一小段水柱,说明装置不漏气。 启普发生器:关闭活塞后,从漏斗注入一定量的水,使漏斗内的水面高于容器内的水面,停止加水后,漏斗中与容器中的液面差保持不再变化,说明启普发生器不漏气。 (三)净化、干燥与反应装置 1、杂质产生原因: (1)反应过程中有挥发性物质,如用盐酸制取的气体中一般有HCl;从溶液中冒出的气体中含有水气。 (2)副反应或杂质参加反就引起,如制乙烯时含SO2;乙炔中的H2S等。 2、装置基本类型:根据净化药品的状态及条件来设计。 图8-7 3、气体的净化剂的选择。 选择气体吸收剂的依据:气体的性质和杂质的性质的差异。主要考虑的是吸收效果,而不是现象。选择一种与杂质反应快而且反应完全的除杂剂。 一般情况下: (1)易溶于水的气体杂质可用水来吸收; (2)酸性杂质可用碱性物质吸收; (3)碱性杂质可用酸性物质吸收; (4)水分可用干燥剂来吸收; (5)能与杂质反应生成沉淀(或可溶物)的物质也可作为吸收剂。 选用吸收剂的原则: (1)只能吸收气体中的杂质,而不能与被提纯的气体反应。 (2)不能引入新的杂质。在密闭装置中进行,要保持装置气体畅通。 4、气体干燥剂的类型及选择。 常用的气体干燥剂按酸碱性可分为三类: (1)酸性干燥剂,如浓硫酸、五氧化二磷、、硅胶。酸性干燥剂能够干燥显酸性或中性的气体,如CO2、SO2、NO2、HCI、H2、Cl2、O2、CH4等气体。 (2)碱性干燥剂,如生石灰、碱石灰、固体NaOH。碱性干燥剂可以用来干燥显碱性或中性的气体,如NH3、H2、O2、CH4等气体。 (3)中性干燥剂,如无水氯化钙等,可以干燥中性、酸性气体,如O2、H2、CH4等。 在选用干燥剂时,显碱性的气体不能选用酸性干燥剂,显酸性的气体不能选用碱性干燥剂。有还原性的气体不能选用有氧化性的干燥剂。能与气体反应的物质不能选作干燥剂,如不能用CaCI2来干燥NH3(因生成CaCl2·8NH3),不能用浓H2SO4干燥NH3、H2S、HBr、HI等。 5、气体净化与干燥装置连接次序。 洗气装置总是进气管插入接近瓶底,出气管口略出瓶塞。干燥管总是大口进,小口出气。 一般情况下,若采用溶液作除杂试剂,则是先除杂后干燥;若采用加热除去杂质,则是先干燥后加热。对于有毒、有害的气体尾气必须用适当的溶液加以吸收(或点燃),使它们变为无毒、无害、无污染的物质。如尾气Cl2、SO2、Br2(蒸气)等可用NaOH溶液吸收;尾气H2S可用CuSO4或NaOH溶液吸收;尾气CO可用点燃法,将它转化为CO2气体。 (四)收集装置 1、设计原则:根据气体的溶解性或密度 (1)易溶或与水反应的气体:用向上(或下)排空气法 (2)与空气成分反应或与空气密度相近的气体:排水(液)法 (3)可溶性气体考虑用排液法 (4)两种方法皆可用时,排水法收集的气体较纯。若欲制取的气体要求干燥,用排空气法或排非水溶剂法。 2、装置基本类型: 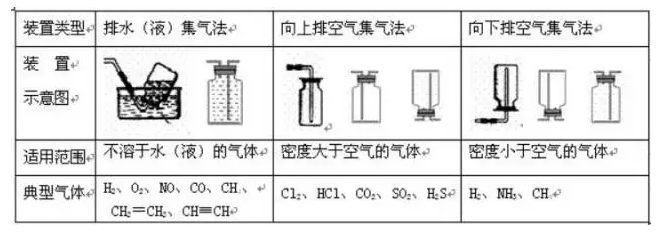 (五)尾气处理装置-安全装置 尾气的处理方法:直接排放、直接吸收、防倒吸吸收、燃烧处理 处理装置: 1、直接吸收 图8-9 2、防止倒吸装置的设计 在某些实验中,由于吸收液的倒吸,会对实验产生不良的影响,如玻璃仪器的炸裂,反应试剂的污染等。因此,在有关实验中必须采取一定的措施防止吸收液的倒吸。防止倒吸一般采用下列措施: (1)切断装置:将有可能产生液体倒吸的密闭装置系统切断,以防止液体倒吸,如实验室中制取氧气、甲烷时,通常用排水法收集气体,当实验结束时,必须先从水槽中将导管拿出来,然后熄灭酒精灯。 (2)置防护装置: ①倒立漏斗式:这种装置可以增大气体与吸收液的接触面积,有利于吸收液对气体的吸收。当易溶性气体被吸收液吸收时,导管内压强减少,吸收液上升到漏斗中,由于漏斗容积较大,导致烧杯中液面下降,使漏斗口脱离液面,漏斗中的吸收液受自身重力的作用又流回烧瓶内,从而防止吸收液的倒吸。下一个装置所示,对于易溶于水难溶于有机溶剂的气体,气体在有机溶剂不会倒吸。 ②肚容式:当易溶于吸收液的气体由干燥管末端进入吸收液被吸收后,导气管内压强减少,使吸收液倒吸进入干燥管的吸收液本身质量大于干燥管内外压强差,吸收液受自身重量的作用又流回烧杯内,从而防止吸收液的倒吸。这种装置与倒置漏斗很类似。 ③蓄液式:当吸收液发生倒吸时,倒吸进来的吸收液被预先设置的蓄液装置贮存起来,以防止吸收液进入受热仪器或反应容器。这种装置又称安全瓶。 ④平衡压强式:为防止分液漏斗中的液体不能顺利流出,用橡皮管连接成连通装置(见恒压式); ⑤防堵塞安全装置式:为防止反应体系中压强减少,引起吸收液的倒吸,可以在密闭装置系统中连接一个能与外界相通的装置,起着自动调节系统内外压强差的作用,防止溶液的倒吸。 ⑥为防止粉末或糊状物堵塞导气管,可将棉花团置于导管口处。 ⑦液封装置:为防止气体从长颈漏斗中逸出,可在发生装置中的漏斗末端套住一只小试管。 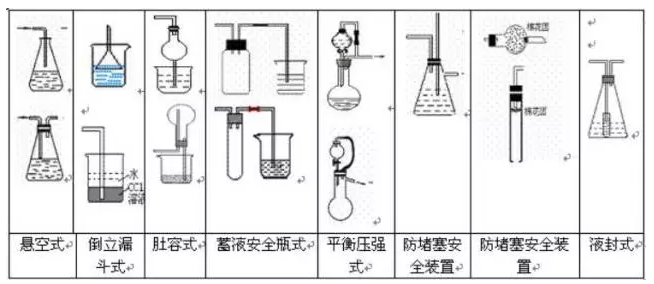 3、防污染安全装置:燃烧处理或袋装 判断原则: (1)有毒、污染环境的气体不能直接排放。 (2)尾气吸收要选择合适的吸收剂和吸收装置。 直接吸收:Cl2、H2S、NO2防倒吸:HCl、NH3、SO2 常用吸收剂:水,NaOH溶液,硫酸铜溶液 (3)可燃性气体且难用吸收剂吸收:燃烧处理或袋装,如CO。 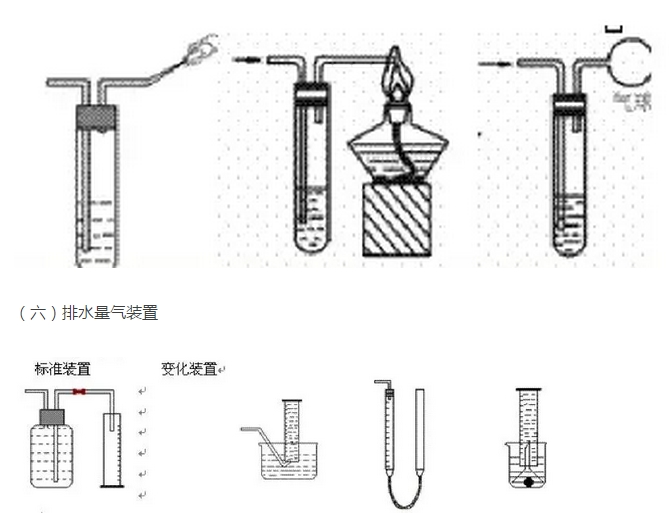 (七)常见气体检验方法 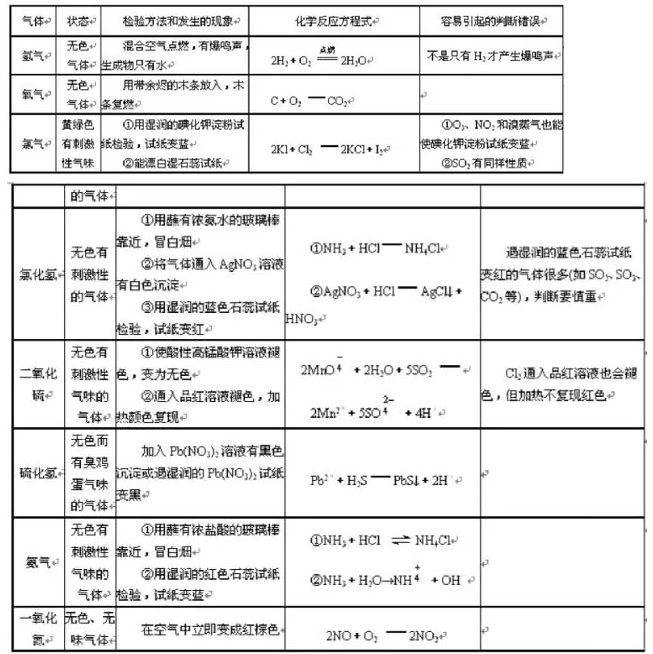 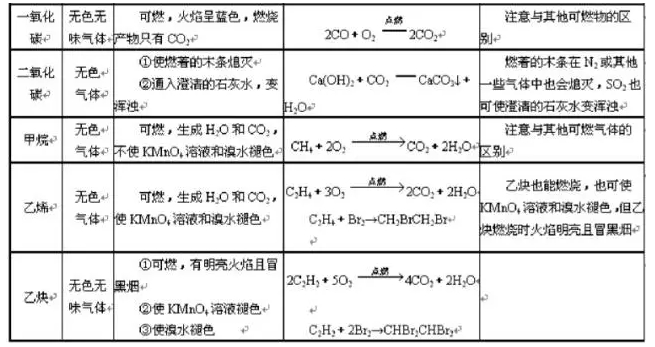 文章来源于网络,由编辑整理,如有侵权请及时联系删除。 (责任编辑:admin) |
