必修一第一章综合练习
http://www.newdu.com 2025/11/06 11:11:27 人民教育出版社 佚名 参加讨论
必修一第一章综合练习 河北衡水市第二中学 薛 杰 1.下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是( ) ① 过滤 ② 蒸发 ③ 溶解 ④ 向容量瓶转移液体 A.①和② B.①和③ C.③和④ D.①和④ 2.下列溶液中Cl-的物质量浓度与50 ml 1mol/LAlCl3溶液中Cl—的物质的量浓度相等的是( ) A.150 mL 2mol/LKCl溶液 B.75 mL 1 mol/LFeCl3溶液 C.150 mL 1 mol/LMgCl2溶液 D.75 mL 3 mol/LCuCl2溶液 3.同温同压下,等质量的SO2和CO2,,正确的叙述是( ) A.分子数之比1:1 B.密度之比4:11 C.密度之比11:16 D.体积之比11:16 4.设NA为阿伏加德罗常数,下列说法正确的是( ) A.在1L 2 mol/L的硝酸镁溶液中含有的硝酸根离子数为NA B.标准状况下22.4L乙醇完全燃烧,生成的二氧化碳的分子数为2NA C.46g二氧化氮(NO2)和46g四氧化二氮(N2O4)含有的原子数均为3NA D.1mol氢氧根离子中含有的电子数为9NA 5.用NA表示阿伏加德罗常数,下列说法不正确 的是 ( ) A.常温常压下,2g氢气所含分子数目为NA B.在标准状况下,NA个水分子所占有的体积约为22.4 L C.18g水中含有的电子数为10NA D.2.4g金属镁变为镁离子时失去的电子数为0.2 NA 6.下列各物质所含原子数目,按由大到小顺序排列的是( ) ①0.5mol NH3 ②标准状况下22.4L He ③4℃ 9mL 水 ④0.2mol H3PO4 A.①④③② B.④③②① C.②③④① D.①④②③ 7. 下列说法正确的是( ) A.CO2的摩尔质量是44g B.阿伏加德罗常数是 0.012kg12C中所含的碳原子数 C.一定温度和压强下,气体的体积主要取决于分子本身的大小 D.物质的摩尔质量等于其相对分子质量 8. 提纯含有少量硝酸钡杂质的硝酸钾溶液,可以使用的方法是( ) A. 加入过量的碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸 B. 加入过量的硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸 C. 加入过量的硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸 D. 加入过量的碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸 9. 下列关于“摩尔”的理解正确的是( ) A. 摩尔是国际科学界建议采用的一种物理量 B. 摩尔是物质的量的单位,简称摩,符号为mol C. 摩尔可以把物质的宏观数量和微观粒子的数量联系起来 D. 国际上规定,0.012kg碳原子所含有的碳原子数目为1mol 10. 某混合气体由一氧化碳和二氧化碳组成,若混合气体在标准状况下的密度是1.875g/L,则混合气体中一氧化碳和二氧化碳的体积比是:( ) A.1:3 B.3:1 C.1:7 D.7:1 11. 物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当他们的体积比为3:2:1时,三种溶液中Cl-离子的物质的量浓度之比是( ) A. 1:1:1 B. 1:2:3 C. 3:2:1 D. 3:4:3 12. 在盛有碘水的试管中,加入少量CCl4后振荡,静置片刻后 ( ) A.整个溶液变紫色 B.整个溶液变为棕黄色 C.上层为无色,下层为紫红色 D.下层无色,上层紫红色 13. 某溶液中含有较大量的Cl-、CO2-3 、OH-等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( ) ①滴加Mg(NO3)2溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液 A.①②④②③ B.④②①②③ C.①②③②④ D.④②③②① 14.在反应X+2Y==R+2M中,已知R和M的摩尔质量之比为22∶9,当1.6 g X和Y完全反应后,生成4.4 g R。则在此反应中Y和M的质量之比为( ) A.16∶9 B.23∶9 C.32∶9 D.46∶9 15. 由硫酸钾、硫酸铝和硫酸组成的混合溶液中,c(H+)=0.1 mol·L-1,c(Al3+)=0.4 mol·L-1,c( SO2-4 )=0.8 mol·L-1,则c(K+)为( ) A.0.15 mol·L-1 B.0.2 mol·L-1 C.0.3 mol·L-1 D.0.4 mol·L-1 16. 将标准状况下的 a L HCl(气体)溶于 1000 g 水中,得到的盐酸的密度为 b g/cm3,则该盐酸的物质的量浓度是( ) A. 17. 下列实验操作或作法正确的是( ) A.用100ml量筒量取8.5ml的水 B.为了不造成浪费,实验剩余的药品放回原瓶 C.把烧杯放在垫有石棉网的铁圈上加热 D.用燃着的酒精灯去点燃另一酒精灯 18.在配制一定物质的量浓度的NaOH溶液时,下列哪个原因会造成所配溶液浓度偏高( )B A.所用NaOH已经潮解 B.向容量瓶中加水未到刻度线 C.有少量NaOH溶液残留在烧杯里 D.定容时观察液面仰视 19. 等体积的NaCl、MgCl2、AlCl3三种溶液分别与等体积等物质和量浓度的AgNO3溶液恰好完全反应,则NaCl、MgCl2、AlCl3三种溶液的物质的量浓度之比是( ) A.1:1:1 B.1:2:3 C.3:2:1 D.6:3:2 20.科学家已发现一种新型氢分子,其化学式为H3,在相同条件下,等质量的H3和H2相同的是( ) A.原子数 B.分子数 C.体积 D.物质的量 21.在相同温度下,相同质量的下列气体分别通入相同容积的密闭容器中,容器内的压强最小的是( ) A.二氧化碳 B.氯气 C.氢气 D.二氧化氮 22.2007年世界十大科技新闻之一是“中国成功发射‘嫦娥一号’卫星”。将来科学家要在月球上进行科学研究,下列实验操作中在月球表面难以完成的是 A.蒸馏 B.溶解 C.过滤 D.蒸发 23..如下图所示,下列实验操作方法正确的是 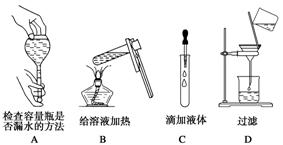 24. 在同温同压下,A容器中的氧气(O2)和B容器中的氨气(NH3)所含的原子个数相同,则A、B两容器中气体的体积之比是 A.1:2 B.2:1 C.2:3 D.3:2 25.已知硫酸溶液的质量分数越大时,其溶液的密度越大,将90%和10%的两种H2SO4溶液等体积混合后,溶液的质量分数为 ( ) A.大于50% B.等于50% C.小于50% D.无法确定 26..已知98%的浓硫酸的浓度为18.4mol.L-1,则49%的硫酸溶液的浓度为( ) A.9.2 mol.L-1 B.大于 9.2 mol.L-1 C.小于 9.2 mol.L-1 D .无法确定 27.某实验小组领取下列仪器(或用品):铁架台(带铁夹、铁圈)、三脚架、石棉网、烧杯、漏斗、分液漏斗、酒精灯、玻璃棒、量筒、蒸发皿、烧瓶、火柴。只应用上述仪器用品。不能进行的实验操作是( ) ①蒸发 ②萃取 ③过滤 ④蒸馏 A.②③ B.①④ C.③④ D.①② 28.设一个12C原子质量为a g,一个R原子质量为b g,阿伏加德罗常数为NA,则R原子的摩尔质量为( ) A. 29.如果1g水中含有a个氢原子,则阿伏加德罗常数应表示为( ) A.9a mol-1 B.18a mol-1 C.9a D.18? 30. 下列说法错误的是 ( ) A.0.3 mol硫酸 B.1 mol水 C.0.5 mol钠 D.1.5 mol氧 31. NA表示阿伏加德罗常数的值,下列关于0.2mol/LK2SO4溶液的说法正确的是 ( ) A.1000mL水中所含K+、SO42-总数为0.3NA B.500mL溶液中含有0.2NA个K+ C.1L溶液中K+的浓度为0.4mol/L D. 1L溶液中SO42-的浓度是0.4mol/L 32.下列实验操作或事故处理中,做法不正确的是 A.不慎将酸溅到眼中,立即用水冲洗,边洗边眨眼睛 B.不慎将浓碱溶液沾到皮肤上,立即用大量水冲洗,然后涂上硼酸溶液 C.不慎碰翻实验桌上燃着的酒精灯失火,马上用湿布扑灭 D.配制硫酸溶液时,先在量筒中加入一定体积的水,再边搅拌边慢慢加入浓硫酸 33.下列溶液中溶质的物质的量浓度为1 mol·L-1的是 A.将40 g NaOH溶解于1 L水中配成的NaOH溶液 B.常温常压下将22.4 L HCl 气体溶于水配成1 L的盐酸溶液 C.将1 L 10 mol/L的浓盐酸与水混合配成10 L溶液 D.从1000 mL 1 mol/L NaCl溶液中取出100 mL的溶液 34. 30mL 1mol/L NaCl溶液和40mL 0.5mol/L CaCl2溶液混合后,混合液中Cl-浓度为( ) A.0.5mol/L B.0.6mol/L C.1.00mol/L D.2mol/L 35. 配制一定体积,一定物质的量浓度的溶液时,下列操作会使溶液的浓度偏高的是( ) A. 容量瓶中原有少量蒸馏水 B. 溶液从烧杯转移到容量瓶中后没有洗涤烧杯 C. 定容时观察液面俯视 D. 定容时倒转容量瓶几次,发现凹液面最低点低于标线,再补几滴水到标线 36.配制0.5 mol·L-1NaOH溶液250 mL,在下列仪器中①托盘天平 ②量筒 ③烧杯 ④玻璃棒 ⑤漏斗 ⑥500 mL容量瓶 ⑦药匙 ⑧250 mL容量瓶 ⑨胶头滴管 ⑩坩埚,需要用到的仪器有( ) A.①③④⑥⑨⑩ B.①④⑦⑧⑨⑩ C.①②③④⑦⑧⑨ D.①②④⑤⑧⑨ 37.用NA表示阿伏加德罗常数的值,下列叙述正确的是( ) A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L B.在常温常压下,11.2L Cl2含有的分子数为0.5NA C.25℃,1.01×105Pa,64gSO2中含有的原子数为3NA D.标准状况下,11.2LH2O含有的分子数为0.5NA 38.两个体积相同的容器,一个盛有一氧化氮,另一个盛有氮气和氧气,在同温同压下两容器内的气体一定具有相同的 A.原子总数 B.质子总数 C.分子总数 D.质量 39. 下列两种气体的分子数一定相等的是 A. 质量相等、密度不等的N2和C2H4 B. 等体积等密度的CO和C2H4 C. 等温等体积的O2和N2 D. 等压等体积的N2和CO2 40.在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是 A. 甲的分子数比乙的分子数多 B. 甲的物质的量比乙的物质的量少 C. 甲的摩尔体积比乙的摩尔体积小 D. 甲的相对分子质量比乙的相对分子质量小 41. 等体积的硫酸铝.硫酸锌.硫酸钠溶液分别与足量氯化钡溶液反应。若生成硫酸钡沉淀的质量比为1:2:3,则三种硫酸盐的物质的量浓度之比为 A.1:2:3 B.1:6:9 C.1:3:3 D.1:3:6 (责任编辑:admin) |