《钠的化合物 》测试
http://www.newdu.com 2025/12/02 04:12:35 人民教育出版社 佚名 参加讨论
《钠的化合物 》测试 重庆四十七中 陈 忆 一、选择题 1.下列物质露置在空气中质量不会增加的是( )。 A.Na2O B.Na2O2 C.Na2CO3 D.NaOH 2.与水作用生成碱并有气体放出的是( )。 A.Na2O B.SiO2 C.Na D.Na2O2 3.下列各组中的两种物质作用时,反应条件或反应物的用量比改变,生成的化合物不会改变的是( )。 A.钠与氧气 B.氢氧化钠与二氧化碳 C.氧化钠与二氧化碳 D.过氧化钠与水反应 4.下列说法正确的是( )。 A.1 g钠投入100 g水中,溶液的总质量为100 g B.1 g表面被氧化的金属钠投入100 g水中,溶液的总质量为101 g C.1 g氧化钠投入100 g水中,溶液的总质量为101 g D.1 g过氧化钠投入100 g水中,溶液的总质量为101 g 5.要除去硫酸钠里混有少量的碳酸钠,应加入的物质是( )。 A.氯化钡溶液B.稀硫酸 C.石灰水 D.氢氧化钠 6.关于NaHCO3的性质,下列说法正确的是( )。 A.和酸反应放出等量的CO2所消耗的酸比Na2CO3少 B.相同温度下溶解度比NaCO3要大 C.热稳定性比Na2CO3小 D.NaHCO3只能和酸作用不能和碱作用 7.将下列固体物质放在空气中,逐渐变成溶液后又变成粉末的是( )。 A.Na2CO3 B.KNO3 C.Na2CO3·10H2O D.NaOH 8.下列离子方程式正确的是( ) A.钠与水反应2Na+2H2O B.氧化钠与盐酸反应 O2-+2H+ C.碳酸氢钠与稀硫酸反应:CO32-+2H+ D.NaOH溶液与小苏打溶液反应 HCO3-+OH- 9.欲除去小苏打溶液中少量的Na2CO3杂质,最易选用加入的物质是( )。 A.干冰B.盐酸 C.碳酸氢钙D.氢氧化钙 10.在天平的两个托盘上,分别放上质量相等的两个烧杯,在烧杯中分别加入等质量的质量分数相等的硫酸,此时天平处于平衡状态,然后分别向两只烧杯中加入等质量的NaHCO3和Na2CO3粉末,待Na2CO3和NaHCO3完全反应,则天平两边( )。 A.放Na2CO3的一端托盘下沉 B.放NaHCO3的端托盘下沉 C.仍保持平衡 D.无法判断 11.由四种不纯的纯碱样品,分别含有下列一种杂质,取等质量的四种样品分别与等质量分数的盐酸反应,所消耗盐酸的质量相等,则这四种样品中含纯碱质量分数最大的是含有杂质( )。 A.NaHCO3 B.KHCO3 C.K2CO3 D.NH4HCO3 12.某容器中通入V L CO2,再加入少量Na2O2后,气体体积缩小到W L,则被吸收的CO2的体积是(均为相同条件下)( )。 A.(V—W)L B.2(V—W)L C.(2V—W)L D.2WL 13.已知NaOH中Na为+1价,对于NaH+H2O A.H2都是还原产物 B.H2都是氧化产物 C.NaH中的氢元素被氧化 D.氧化产物与还原产物质量相等 14.在一定温度下,向饱和Na2CO3溶液中加入1.06 g无水Na2CO3,搅拌后静置,最终所得晶体的质量为( )。 A.等于1.06 g B.大于2.86 g C.等于2.86 g D.大于1.06 g小于2.86 g 15.在下列反应中,Na2O2只表现出强氧化性的是( ) A.2Na2O2+CO2 B.Na2O2+MnO2 C.2Na2O2+H2SO4 D.5Na2O2+2MnO4-+16H+ 16.将质量比等于式量比的Na、Na2O、Na2O2、NaOH,分别投入等质量的足量水中,所得溶液质量分数最大的是( )。 A.Na B.Na2O C.Na2O2 D.NaOH 17.在某碱性溶液中可以大量共存的离子组是( )。 A.Na+、CO32-、K+、NO3- B.Na2+、K+、Cl-、NO3- C.Mg2+、K+、SO42-、Cl- D.Ba2+、Na+、SO32-、Cl- 18.金属钠与其在空气中燃烧产物x分别加入到足量水中,生成的两种气体在一定条件下恰好完全反应,则与水反应的金属钠与被氧化成x的金属钠的质量比( )。 A.1:1 B.2:1 C.23:78 D.46:78 19.下列反应中,一种物质既作氧化剂,又作还原剂的是( )。 A.2Na+2H2O B.2H2O C.2Na2O2+2H2O D.2F2+2H2O 20.下列物质混合后溶液中溶质的质量分数最大的是( )。 A.4.6 g钠投入45.4 g水中 B.6.2 g氧化钠投入42.2 g水中 C.7.8 g过氧化钠投入42.2 g水中 D.8 g烧碱投入42 g水中 二、填空题 21.Na2O是 色固体,与水反应的化学方程式为 ,制取Na2O通常采用的方法是2NaNO2+6Na 22.填写出有关物质的化学式 (1)医药上用作缓泻剂的是 (2)可用来漂白织物、麦杆、羽毛的是 (3)用于制电光源的是 (4)用作原子反应堆导热剂的是 (5)用于玻璃、制皂、造纸、纺织等工业上的是 (6)用于焙制糕点的发酵粉及治疗胃酸过多的药剂的是 23.如果不慎将浓NaOH溶液洒在皮肤上,应马上 24.氢氧化钠又称 、 或 ,它极易溶于水,且 ,在空气中易吸收水蒸气,而发生 ,因此,氢氧化钠可作为一些气体的 ,对它必须 保存,且瓶塞要用 。 25.将CO2通入饱和Na2CO3溶液中,会发生 现象,这说明 ,有关反应的离子方程式为 。 三、推断题 26.A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按图所示关系相互转化,已知A为单质。 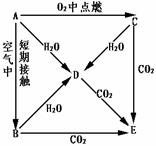 (1)写出A→E的化学式: (1)写出A→E的化学式:A B C D E (2)写出A→D、C→D、C→E反应的化学方程式 A→D: C→D: C→E: 四、计算题 27.将7.8 g Na2O2投入到100 g 10%的苛性钠溶液中充分反应。求: (1)所得溶液的质量分数 (2)向该溶液中通入一定量CO2,然后小心蒸干,所得固体冷却干燥,称重为58.8 g,通过计算推出该固体物体的组成和质量。 28.加热一定量的小苏打充分反应后,称量剩余物A发现比原来少了3.1 g。若加热同质量的小苏打及一定量的Na2CO3·xH2O的混合物,充分反应后,称量乘余物B,发现比原来减少12.1 g。又知剩余物的质量比是B:A=2:1。求x的值。 参考答案 一、1.C2.CD3.CD4.C5.B6.AC7.D8.AD9.A10.A 11.B12.B13.CD14.B15.B16.BC17.AB18.A19.BC20.BC 二、21.白,Na2O+H2O 22.(1)Na2SO4·10H2O(2)Na2O2(3)Na(4)NaK合金(5)Na2CO3(6)NaHCO3 23.用大量水冲洗24.略25.白色沉淀,NaHCO3比Na2CO3溶解度小 2Na++CO2+H2O+CO32- 三、26.(1)Na、Na2O、Na2O2、NaOH、Na2CO3,(2)2Na+H2O 2Na2O2+2H2O 2Na2O2+2CO2 四、27.(1)17% (2)NaHCO3 12.6gNa2CO3 15.9g 28.x=10 (责任编辑:admin) |