2018高考化学冲刺,电离平衡常数及其应用知识总结
http://www.newdu.com 2025/10/28 11:10:37 三好网 佚名 参加讨论
2018高考化学备考过程中,很多同学感到化学知识点多,记起来很吃力。但是,如果将一些知识点总结起来,形成脉络体系,综合记忆,就会容易很多。小编将2018高考化学冲刺,电离平衡常数及其应用知识总结如下:  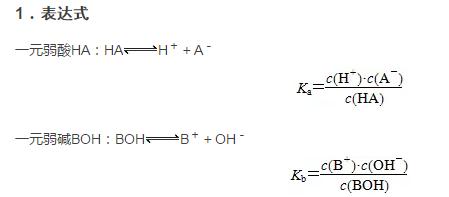 2.特点 (1)电离常数只与温度有关,升温,K值增大。 (2)多元弱酸的各级电离常数的大小关系是K1?K2?K3,故其酸性取决于第一步电离。 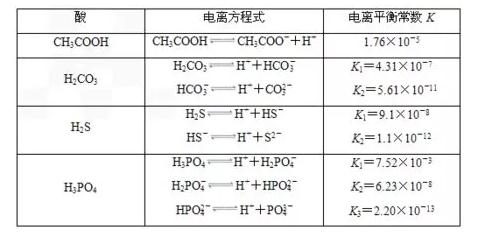 3.意义 根据酸碱的电离常数大小可进行以下判断: (1)判断弱酸(或弱碱)的相对强弱,电离常数越大,酸性(或碱性)越强。 例如,已知在相同温度下,三种酸的电离常数如下表,根据表中电离常数大小关系,则酸性排序为HZ>HY>HX。 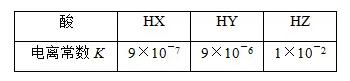 (2)判断盐溶液的酸性(或碱性)强弱,电离常数越大,对应的盐水解程度越小,碱性(或酸性)越弱。 (3)判断复分解反应能否发生,一般符合“强酸制弱酸”规律。 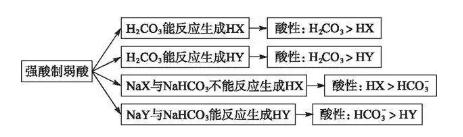 (4)判断微粒浓度比值的变化。 弱电解质加水稀释时,能促进弱电解质的电离,溶液中离子和分子的浓度会发生相应的变化,但电离常数不变,考题中经常利用电离常数来判断溶液中微粒浓度比值的变化情况。  文章来源于网络,由编辑整理,如有侵权请及时联系删除。 (责任编辑:admin) |