2018高考有机化学二轮复习有机合成推断知识点
http://www.newdu.com 2025/12/02 09:12:28 三好网 佚名 参加讨论
2018年高考二轮复习是高考成绩提升的关键期,考生一定要积极备考,梳理高中学科知识脉络,牢记知识点。小编整理了2018高考有机化学二轮复习知识点,有机合成推断知识总结如下:  Q:什么是有机合成? A:有机合成是利用简单、易得的原料,通过有机反应,生成具有特定结构和功能的有机化合物。 Q:有机合成的任务有那些? A:有机合成的任务包括目标化合物分子骨架构建和官能团的转化。 Q:用示意图表示出有机合成过程。 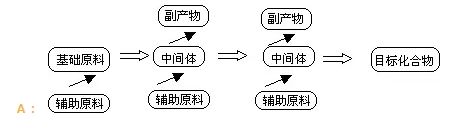 1.有机合成中碳骨架的构建 (1)链增长的反应 ①加成反应(加聚反应) ②缩聚反应 ③酯化反应等 (2)链减短的反应 ①烷烃的裂化反应 ②烯烃、炔烃的氧化 ③羧酸盐脱羧基成CO2 ④水解反应(酯类、糖类、蛋白质等) (3)常见由链成环的方法 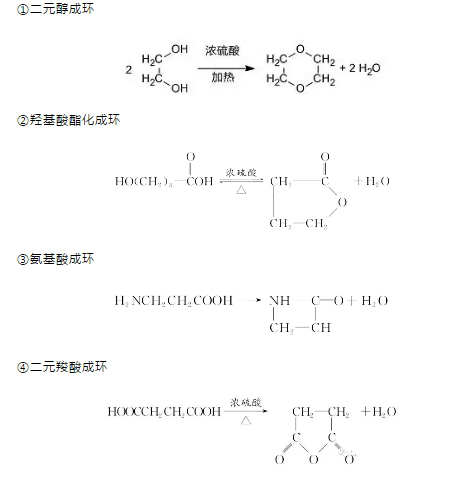 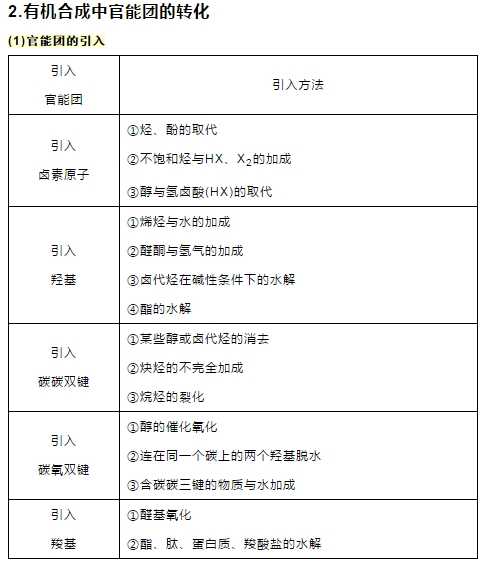 (2)官能团的消除 ①通过加成反应消除不饱和键(双键、三键、苯环) ②通过消去、氧化或酯化反应等消除羟基 ③通过加成或氧化反应等消除醛基 ④通过水解反应消除酯基、肽键、卤素原子 (3)官能团的改变(利用官能团的衍生关系) 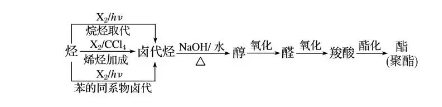 (4)有机合成中官能团的保护 ①酚羟基的保护 因酚羟基易被氧化,所以在氧化其他基团前可以先使其与NaOH反应,把—OH变为—ONa将其保护起来,待氧化后再酸化将其转变为—OH。 ②碳碳双键的保护 碳碳双键也容易被氧化,在氧化其他基团前可以利用其与HCl等的加成反应将其保护起来,待氧化后再利用消去反应转变为碳碳双键。 ③氨基(—NH2)的保护 如在对硝基甲苯对氨基苯甲酸的过程中应先把—CH3氧化成—COOH之后,再把—NO2还原为—NH2,防止当KMnO4氧化—CH3时,—NH2(具有还原性)也被氧化。 3.有机合成题的解题思路 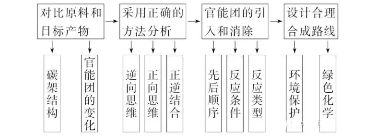 (1)有机合成的分析方法 ①正向合成分析法 基础原料―→中间体―→目标化合物 ②逆向合成分析法 目标化合物―→中间体―→基础原料 (2)有机合成遵循的原则 ①起始原料要廉价、易得、低毒性、低污染。 ②应尽量选择步骤最少的合成路线。 ③合成路线要符合“绿色、环保”的要求。 ④有机合成反应要操作简单、条件温和、能耗低、易于实现。 ⑤要按一定的反应顺序和规律引入官能团,不能臆造不存在的反应。 (3)依据特征结构、性质及现象推断 根据试剂或特征现象推知官能团的种类 ①使溴水褪色,则表示该物质中可能含有“”或“”结构。 ②使KMnO4(H+)溶液褪色,则该物质中可能含有“”、“”或“—CHO”等结构或为苯的同系物。 ③遇FeCl3溶液显紫色,或加入溴水出现白色沉淀,则该物质中含有酚羟基。 ④遇浓硝酸变黄,则表明该物质是含有苯环结构的蛋白质。 ⑤遇I2变蓝则该物质为淀粉。 ⑥加入新制的Cu(OH)2悬浊液,加热煮沸有砖红色沉淀生成或加入银氨溶液加热有银镜生成,表示含有—CHO。 ⑦加入Na放出H2,表示含有—OH或—COOH。 ⑧加入NaHCO3溶液产生气体,表示含有—COOH。 根据反应条件推断反应类型 ①在NaOH的水溶液中发生水解反应,可能是酯的水解反应也可能是卤代烃的水解反应。 ②在NaOH的乙醇溶液中加热,发生卤代烃的消去反应。 ③在浓H2SO4存在的条件下加热,可能发生醇的消去反应、酯化反应、成醚反应或硝化反应等。 ④能与溴水或溴的CCl4溶液反应,可能为烯烃、炔烃的加成反应。 ⑤能与H2在Ni作用下发生反应,则为烯烃、炔烃、芳香烃、醛、酮的加成反应或还原反应。 ⑥在O2、Cu(或Ag)、加热(或CuO、加热)条件下,发生醇的氧化反应。 ⑦与O2或新制的Cu(OH)2悬浊液或银氨溶液反应,则该物质发生的是 —CHO的氧化反应。(如果连续两次出现O2,则为醇―→醛―→羧酸的过程) ⑧在稀H2SO4加热条件下发生酯、低聚糖、多糖等的水解反应。 ⑨在光照、X2(表示卤素单质)条件下发生烷基上的取代反应;在Fe粉、X2条件下发生苯环上的取代反应。 根据有机反应中定量关系进行推断 ①烃和卤素单质的取代:取代1 mol 氢原子,消耗1 mol 卤素单质(X2)。 ②碳碳双键的加成:与H2、Br2、HCl、H2O等加成时按物质的量比1∶1加成。 ③含—OH的有机物与Na反应时:2 mol —OH生成1 mol H2。 ④1 mol —CHO对应2 mol Ag;或1 mol —CHO对应1 mol Cu2O。 ⑤物质转化过程中相对分子质量的变化 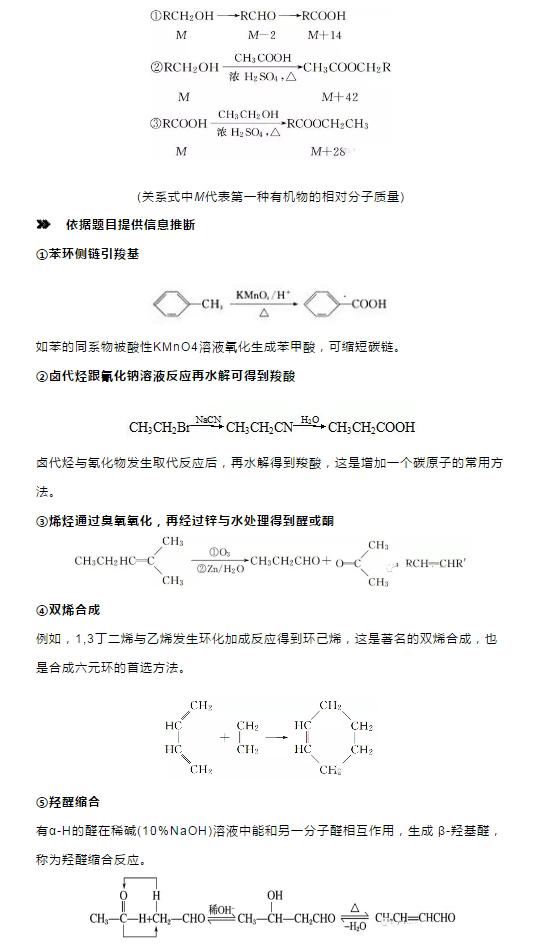 文章来源于网络,由编辑整理,如有侵权请及时联系删除。 (责任编辑:admin) |