人教版高二化学选修1,合金知识考点总结
http://www.newdu.com 2025/11/21 01:11:40 三好网 佚名 参加讨论
人教版高二化学选修1,合金知识考点总结,包含营养平衡能源物质与合金生活材料物质等。在高考中,这块知识出大题可能性不大,可能会出一些小的选择题目。面对考试,每一分都要争取,所以高中化学家教老师整理出人教版高二化学选修1,合金知识考点总结如下:  合金的概念: 合金是在金属中加热熔合某些金属或非金属形成的具有金属特性的物质。 ①合金可以是金属与金属或金属与非金属的混合物,不一定全部由金属组成。 ②合金具有金属特性,如导电性、导热性、延展性等。 ③合金是几种成分熔合在一起形成的,发生的是物理变化,不是化学变化;合金不是几种成分简单地混合而成的。 ④合金中各成分仍保持自己的性质。 合金与组成它们的金属的性质比较: 金属熔合了其他金属或非金属后,不仅组成上发生了变化,其内部结构也发生了改变,从而引起性质的变化。因而合金比纯金属具有更广泛的用途。 纯金属与合金性质的比较: ①合金一般比其组分金属的颜色更鲜艳。 ②合金的硬度一般应工组成它的金属。 ③合金的熔点一般低于成它的金属。 ④合金的抗腐蚀能力一般强工组成它的金属。 ⑤合金的导电性、导热隆能一般差于组成它的金属。 生铁和钢的比较: 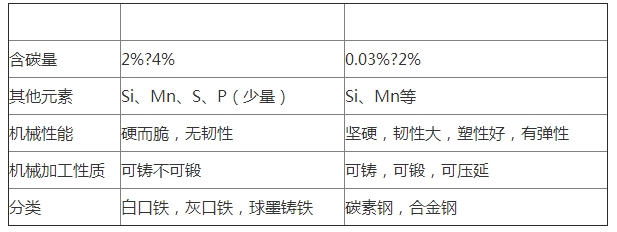 知识点拨: ①生铁和熟铁:生铁是指含碳债在 2%一4.3%之间的铁合金,熟铁是用生铁精炼而成的较纯的铁,含碳量低于0.02%。 ②生铁与铸铁:铸铁是生铁中的一种,是指可用来铸造的生铁,通常指球墨铸铁。 ③碳素钢的性能与含碳址有关,含碳量越高,硬度越大,但韧性越差;含碳量越低,韧性越好,但硬度越小。 ④纯铁与日常生活中铁的颜色差异日常生活,我们接触的铁一般不是纯铁,而是一些铁的氧化物或含铁的混合物,故我们常见的铁的颜色是黑色的,但它并不是纯铁的颜色,纯铁的颜色是银白色的。 应用广泛的合金: (1)铁合金:铁合金包括生铁和钢,生铁和钢的主要成分是铁,钢与生铁的各种性能不同,主要是由于二者的含碳量不同。 生铁与钢的种类 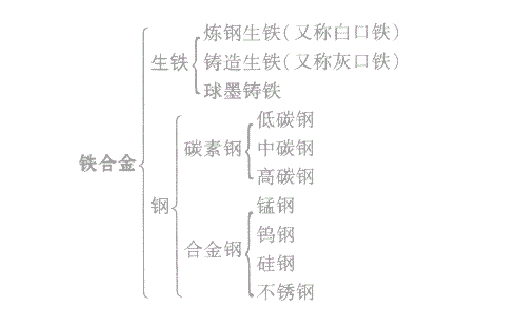 (2)生铁与钢: 生铁的含碳量为2%?4.3% 钢的含碳量为0.03%?2% (3)钛和钛合金:钛和钛合金被认为是21世纪的重要金属材料。 ①性质:优异的耐腐蚀性,对海水、空气和若干腐蚀介质都稳定,可塑性好,强度大,密度小,又称亲生物金属; ②用途:喷气发动机、飞机.机身、人造卫星外壳、火箭壳体、医学补形、人造骨、海水淡化设备、海轮和舰艇的外壳等。 概述: 金属是一种具有光泽(即对可见光强烈反射)、富有延展性、容易导电、导热等性质的物质。金属的上述特质都跟金属晶体内含有自由电子有关。在自然界中,绝大多数金属以化合态存在,少数金属例如金、铂、银、铋以游离态存在。金属矿物多数是氧化物及硫化物。其他存在形式有氯化物、硫酸盐、碳酸盐及硅酸盐。金属之间的连结是金属键,因此随意更换位置都可再重新建立连结,这也是金属伸展性良好的原因。金属元素在化合物中通常只显正价。 金属物理性质的共性: 大多数金属在常温下是固体,具有金属光泽,是电和热的良导体,具有良好的延展性,密度较大,熔沸点较高。 金属物理性质的特性: 不同的金属有其各自的特性。如铁、铝等大多数金属都呈银白色,但铜呈红色,金呈黄色;常温下,铁、铝、铜等大多数金属都是固体,但汞是液体;不同金属的导电性、导热性、密度、熔点、硬度等物理性质差别也较大,见下表。 jjjjj3 用途: 钛和钛的合金:可用于制造喷气发动机,轮船外壳,反应器和电信器材。 锌:锌镀在铁的表面,以防止铁被腐蚀;锌还常用于电镀、制造铜合金和干电池。 铜:制造电线、电缆和各种电器。 铝:来冶炼高熔点金属;导电性仅次于银和铜,常用于制造电线和电缆。 物质的性质和用途的关系: ①物质的性质在很大程度上决定了物质的用途,但实际运用时,还需要考虑价格、资源、是否美观、使用是否便利,以及废料是否易于回收和对环境的影响等多种因素。 ②应用举例 a.日常生活中菜刀、镰刀、锤子等用铁制而不用铅制,这是因为铁的硬度比铅大,并且铅对人体有害。 b.虽然银的导电性比铜好,但由于银的价格比铜高得多,所以电线一般用铜制而不用银制。 c.灯泡里的灯丝用钨制而不用锡制,这是因为钨是熔点最高的金属,高温时钨丝不易熔化;而锡的熔点最低 (只有232℃),如果用锡制灯丝,只要一开灯,灯丝就会断开,灯泡不能发光。 d.铁制水龙头要镀铬,这是因为镀铬既美观,又耐腐蚀,可延长水龙头的使用寿命。 e.在日常生活中我们还经常用到其他金属,如温度计中的液态金属汞、干电池的锌皮、热水瓶内胆上镀的金属银等。 定义: 金属材料是指金属元素或以金属元素为主构成的具有金属特性的材料的统称。 常见的金属材料包括: 纯金属、合金、金属材料金属间化合物和特种金属材料等。 (注:金属氧化物(如氧化铝)不属于金属材料) 几种重要的金属: (1)铁(Fe) 纯铁具有银白色金属光泽,质软,有良好的延展性,是电和热的良导体,密度为7.86g/cm3,属重金属,熔点为1535℃,中考,沸点为2750℃。 (2)铝(Al) 具有银白色金属光泽,密度为2.70g/cm3,熔点为660℃,沸点为2200℃。具有良好的延展性、导电性和一导热性。在空气中,铝表面能形成一层致密的氧化物薄膜,可阻止铝进一步被氧化;铝对浓硝酸等有耐腐蚀性;在高温时还原性很强,可川来冶炼高熔点金属;导电性仅次于银和铜,常用于制造电线和电缆。 (3)铜(Cu) 具有红色金属光泽,密度为8.92g/cm3,熔点为1083℃,沸点为2595℃。具有良好的延展性、导电性和导热性。铜在干燥的空气中化学性质不活泼,在潮湿的空气中,表面可生成碱式碳酸铜(铜绿);导电性在金属中仅次于银,用于制造电线、电缆和各种电器。 (4)锌(Zn) 具有青白色金属光泽,密度为7.14g/cm3,熔点为419.4℃,沸点为907℃.锌在空气中比较稳定,在表面能形成一层致密的氧化物薄膜,所以常将锌镀在铁的表面,以防止铁被腐蚀;锌还常用于电镀、制造铜合金和干电池。 (5)钛(Ti)具有银白色金属光泽,密度为4.5g/cm3,熔点为1725℃,沸点为3260℃。具有良好的延展性和耐腐蚀性。钛和钛的合金可用于制造喷气发动机,轮船外壳,反应器和电信器材。 人类使用金属的历史: 人类最早使用的金属制品是青铜器,然后过渡到铁器时代,再后就是铝制品时代。人类使用金属的历史主要与金属的活动性及冶炼技术的难易有关。 金属之最: (])地壳中含量最多的金属元素?铝(Al) (2)人体中含量最高的金属元素?钙(Ca) (3)导电、导热性最好的金属?银(Ag) (4)熔点最高的金属?钨(W) (5)目前世界年产址最高的金属?铁(Fe) (6)硬度最大的金属?铬(Cr) (7)密度最大的金属?饿(Os) (8)密度最小的金属?铿(Li) 金属材料的分类: 金属材料可分为黑色金属材料和有色金属材料。黑色金属材料通常包括铁、铬、锰以及它们的合金,是应用最广泛的金属材料,除黑色金届外其他各种金属称为有色金属。 纯金: 在欧洲和美洲,把纯金叫做“24K","18K”金就是含黄金18份,其余的6份是铜,合为成数,就是七成五。把成数和K数互相折合,可以用下边两个公式:成数÷10×24=K数,K数÷24×10=成数。美国的金元按规定是21.6K,用上面的公式一算,可以知道应该用九成金来铸。普通的金表外壳和金笔尖都是14K,你可以算一算是几成金。 相关您感兴趣的高中化学知识点内推荐: 人教版高二化学选修1,生命基础能源糖类知识考点总结 人教版高二化学选修1,重要体内能源油脂知识考点总结 人教版高二化学选修1,生命基础蛋白质知识考点总结 人教版高二化学选修1,改善大气质量知识考点总结 人教版高二化学选修1,垃圾资源化知识考点总结 人教版高二化学选修1,玻璃陶瓷水泥知识考点总结 人教版高二化学选修1,塑料纤维和橡胶知识考点总结 人教版高二化学选修1,合金知识考点总结 人教版高二化学选修1,爱护水资源知识考点总结 人教版高二化学选修1,金属腐蚀和防护知识考点总结 (责任编辑:admin) |