高二化学选择性必修1,第二章第一节化学反应速率
http://www.newdu.com 2025/12/01 01:12:03 三好网 佚名 参加讨论
下面是高中化学老师给大家带来高二化学选择性必修1,第二章第一节化学反应速率的知识要点,希望能帮到大家。  第一节化学反应速率 [核心素养发展目标] 1.变化观念:了解化学反应速率的概念及其表示方法,形成不同的反应可用不同的方法来表示化学反应速率的变化观念。 2.证据推理:根据化学反应速率的测定原理,设计实验学会化学反应速率的测定方法,通过对比的方法,发展基于变量关系的证据推理素养。 一、化学反应速率及其表示方法 1.化学反应速率的概念及其数学表达式 (1)概念:化学反应速率是定量描述化学反应进行快慢程度的物理量。通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示。 (2)数学表达式为:v=Δc/Δt或v=Δn/(v·Δt)。 (3)单位常用mol·L-1·s-1或mol·L-1·min-1表示。 2.化学反应速率与化学计量数之间的关系 (1)在一个容积为2L的密闭容器中充入一定物质的量的SO2和O2,则发生反应: 2SO2+O2?2SO3, 经5s后,测得SO3的物质的量为0.8mol,填写下表: 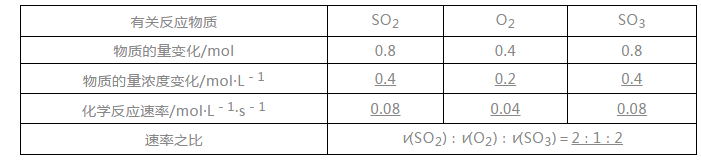 (2)分析上表可知 ①一般来说,随着反应的逐渐进行,反应物浓度会逐渐减小,化学反应速率也会逐渐减慢。因此,化学反应速率通常是指某一段时间内的平均反应速率,而不是瞬时反应速率。 ②在同一化学反应中,选用不同物质表示化学反应速率,其数值可能相同也可能不相同,但表示的意义相同。因此,表示化学反应速率时,必须指明用哪种物质作标准,在速率v的后面将该物质的化学式用括号括起来。 ③用不同反应物表示化学反应速率时,化学反应速率之比=物质的量浓度变化量之比=物质的量变化量之比=化学计量数之比。 3.例题 例1反应:4A(s)+3B(g)=2C(g)+D(g),经2min后,B的浓度减少0.6mol·L-1。对此反应速率的表示正确的是() A.用A表示的反应速率是0.4mol·L-1·min-1 B.分别用B、C、D表示的反应速率之比是3∶2∶1 C.在2min末的反应速率,用B表示是0.3mol·L-1·min-1 D.在2min内的反应速率,用C表示是-0.2mol·L-1·min-1 答案B 解析化学反应速率是一段时间内的平均反应速率,不是瞬时反应速率,只能取正值;不能用固体或纯液体表示某一反应的反应速率。 例2反应A(g)+3B(g)?2C(g)+2D(g)在四种不同情况下的反应速率分别为 ①v(A)=0.15mol·L-1·min-1 ②v(B)=0.01mol·L-1·s-1 ③v(C)=0.40mol·L-1·min-1 ④v(D)=0.45mol·L-1·min-1 则该反应在不同情况下进行的快慢顺序为。 答案④>③=②>① 解析将以不同物质表示的反应速率换算为用同一物质同一单位表示的速率,再比较速率数值的大小。若以物质A为标准,根据用不同物质表示同一反应的速率时,速率之比等于各物质的化学计量数之比,将②③④的反应速率换算为用物质A表示的反应速率。 二、化学反应速率的测定 1.测定原理 利用与化学反应中任何一种化学物质的浓度(或质量)相关的性质进行测定。 2.测定方法 (1)直接观察测定:如释放出气体的体积和体系的压强等。 (2)科学仪器测定:如反应体系颜色的变化。在溶液中,当反应物或产物本身有较明显的颜色时,可利用颜色深浅和显色物质浓度间的正比关系来跟踪反应的过程和测量反应速率。 3.实验测定化学反应速率 设计实验测定锌与硫酸反应的速率,按下列实验步骤完成实验: (1)按下图所示安装装置,加入锌粒,然后快速加入40mL1mol·L-1的硫酸,测量收集10mL氢气所用的时间。 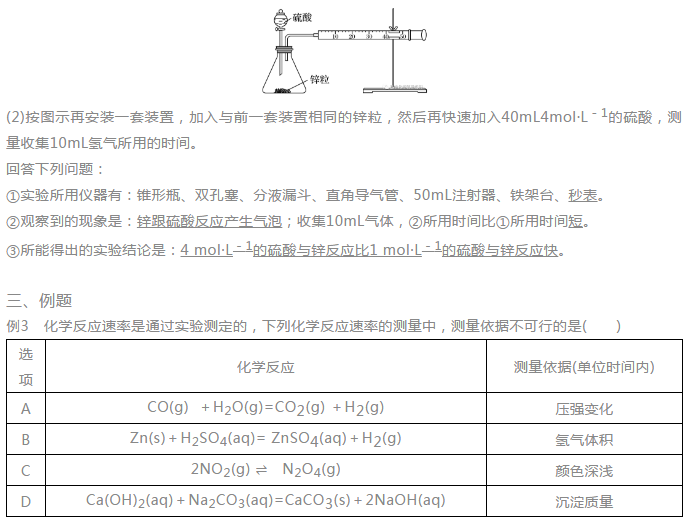 答案A 解析 化学反应速率用单位时间内反应物浓度的减少或生成物浓度的增加来表示。A项,该反应是气体分子数不变的反应,反应前后压强不变; B项,单位时间内H2体积变化大,速率快;C项,2NO2?N2O4,NO2是红棕色气体,N2O4是无色气体,可以用单位时间内气体颜色的变化来衡量反应的快慢; D项,单位时间内产生沉淀的质量越多,速率越快。 四、当堂练 1.(2018·沈阳调研)下列有关化学反应速率的说法中正确的是() A.对任何化学反应来说,反应速率越大,反应现象就越明显 B.化学反应速率通常用单位时间内任何一种反应物浓度的减少或任何一种生成物浓度的增加来表示 C.若某化学反应的反应速率为0.5mol·L-1·s-1,就是指在该时间内反应物和生成物的浓度变化都为0.5mol·L-1·s-1 D.化学反应速率是用来衡量化学反应进行快慢的物理量 答案D 解析A项,中和反应速率很快,但有的没有明显现象,错误;B项,在化学反应中,由于固体和纯液体的浓度视为常数,其浓度变化值为零,故不能用它们表示反应速率,错误;C项,单位错,浓度变化单位应为mol·L-1,且由于化学计量数不一定相同,在该时间内反应物和生成物的浓度变化不一定都为0.5mol·L-1。 2.对于化学反应: 3W(g)+2X(g)=4Y(g)+3Z(g) 下列反应速率关系中,正确的是() A.v(W)=3v(Z)B.2v(X)=3v(Z)C.2v(X)=v(Y)D.3v(W)=2v(X) 答案C 解析对于任一化学反应,用不同的物质表示该反应的速率,其数值之比等于其化学计量数之比,v(W)∶v(X)∶v(Y)∶v(Z)=3∶2∶4∶3,C正确。 3.在铝与稀硫酸的反应中,已知10s末硫酸的浓度减少了0.6mol·L-1,若不考虑反应过程中溶液体积的变化,则10s内生成硫酸铝的平均反应速率是() A.0.02mol·L-1·min-1B.1.8mol·L-1·min-1 C.1.2mol·L-1·min-1D.0.18mol·L-1·min-1 答案C 解析 v(H2SO4)=0.6mol·L-1/10s=0.06mol·L-1·s-1, v[Al2(SO4)3]=0.06mol·L-1·s-1/3=0.02mol·L-1·s-1×60s·min-1=1.2mol·L-1·min-1。 4.一定条件下,向2L密闭容器中加入2molN2和10molH2,发生反应: N2(g)+3H2(g)?2NH3(g), 2min时测得剩余N21mol,下列化学反应速率不正确的是() A.v(N2)=0.25mol·L-1·min-1B.v(H2)=0.75mol·L-1·min-1 C.v(NH3)=1mol·L-1·min-1D.v(NH3)=0.5mol·L-1·min-1 答案C 五、课后练 题组一化学反应速率及其数学表达式的应用 1.下列关于化学反应速率的说法,不正确的是() A.化学反应速率是衡量化学反应进行快慢程度的物理量 B.化学反应速率的大小主要取决于反应物的性质 C.化学反应速率可以用单位时间内生成某物质的质量的多少来表示 D.化学反应速率常用单位有mol·L-1·s-1和mol·L-1·min-1 答案C 解析化学反应速率用单位时间内反应物或生成物的浓度变化量来表示,而不采用物质的质量或物质的量。 2.用纯净的碳酸钙与1mol·L-1100mL稀盐酸反应制取二氧化碳。关于此反应,下列说法不正确的是() A.可以用单位时间内碳酸钙质量的减少表示该反应的反应速率 B.可以用单位时间内生成二氧化碳的量表示该反应的反应速率 C.可以用单位时间内溶液中Ca2+浓度的增加表示该反应的反应速率 D.可以用单位时间内碳酸钙浓度的变化表示该反应的反应速率 答案D 解析CaCO3为固体,浓度不变化。 3.在2L密闭容器内,某气体反应物在2s内由8mol变为7.2mol,则用该气体表示该反应的平均反应速率为() A.0.4mol·L-1·s-1B.0.3mol·L-1·s-1 C.0.2mol·L-1·s-1D.0.1mol·L-1·s-1 答案C 解析v=(8mol-7.2mol)/2L/2s=0.2mol·L-1·s-1。 题组二化学反应速率与化学计量数关系的应用 5.(2018·咸阳高二质检)在一个密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8mol·L-1和5.4mol·L-1,在一定条件下反应生成NH3,10min后测得N2的浓度是0.8mol·L-1,则在这10min内NH3的平均反应速率是() A.0.1mol·L-1·min-1B.0.2mol·L-1·min-1 C.0.3mol·L-1·min-1D.0.6mol·L-1·min-1 答案B 6.反应:3X(g)+Y(g)?2Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.5mol,则此反应的反应速率为() A.v(X)=0.05mol·L-1·min-1B.v(Y)=0.10mol·L-1·min-1 C.v(Z)=0.10mol·L-1·min-1D.v(W)=0.10mol·L-1·s-1 答案C 7.(2018·山西运城月考)在密闭容器中A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示。已知v(A)、v(B)、v(C)之间有以下关系:2v(B)=3v(A)=3v(C)。则此反应可表示为() A.2A+3B=2CB.A+3B=2C C.3A+B=2CD.A+B=C 答案A 解析根据2v(B)=3v(A)=3v(C)可知,v(A)∶v(B)∶v(C)=2∶3∶2,A项正确。  题组三化学反应速率图像分析 8.一定温度下,在0.5L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,10s时达到化学平衡状态。则从反应开始到10s末的反应速率用X表示是()  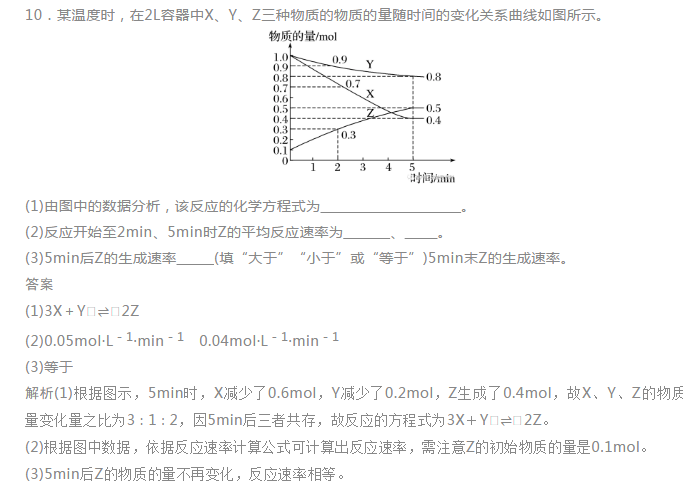 声明: (责任编辑:admin) |