妙解化学平衡题
http://www.newdu.com 2025/12/02 10:12:33 人民教育出版社 佚名 参加讨论
妙解化学平衡题 黑龙江省大庆市第五十六中学 卢国锋 一、特征法 对题干和选择支的特点进行分析,发现隐含信息,得出正确判断的方法。 例1.在一个不导热的密闭反应器中,只发生两个反应: a(g)+b(g) A.等压时,通入惰性气体,c的物质的量不变 B.等压时,通入z气体,反应器中温度升高 C.等容时,通入惰性气体,各反应速率不变 D.等容时,通入z气体,y的物质的量浓度增大 妙法点拨:看题设的特征再看选项,题设不导热的密闭反应器,选项研究恒容和恒压下的变化,这与反应物与生成物的聚集状态和化学计量数有关,前一个反应化学计量数不变,压强对它没有影响,等压时,通入惰性气体,相当于减压,后一反应平衡向逆反应方向移动,放出热量温度升高,前一反应平衡向逆反应方向移动,c的物质的量变化。答案(A)。 二、假设法 当某一可变因素的存在形式限定在有限种可能时,假设该因素处于某种情况,并以此为条件进行推理。 例2.在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g) 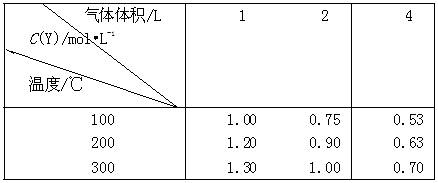 下列说法不正确的是 A.m<n B.Q<0 C.温度不变,压强增大,Y的质量分数减小 D.体积不变,温度升高,平衡向正反应方向移动 妙法点拨:横向观察表中数据可知,当温度不变,将容积的体积扩大1倍时,假设平衡不移动应该为0.5mol/L、0.6mol/L、0.65mol/L,而平衡后的生成物Y的浓度大于原来的1/2,说明降低压强平衡向正反应方向移动,即m小于n。增大压强平衡向逆反应方向移动,生成物Y的质量分数减小;纵向观察表中数据可知,当压强不变时,升高温度,生成物Y的浓度是增大的,说明升高温度平衡向正反应方向移动,则反应是吸热反应,即Q大于0。答案(B)。 三、比较法 有比较才有鉴别,对比各个事物或现象,以揭示它们之间共同点和差异点的思维方法,解题过程是寻找联系和区别的过程。 例3.相同容积的四个密闭容器中进行同样的可逆反应:2X(g)+Y(g) A.X的转化率为:甲<丙<乙<丁 B.X的转化率为:甲<乙<丙<丁 C.Y的转化率为:甲>丙>乙>丁 D.Y的转化率为:丁>乙>丙>甲 妙法点拨:将起始时情况作如下排列: 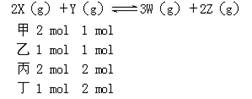 甲与乙比较,甲相当于在乙的基础上再增加X的物质的量,甲中Y的转化率大于乙中Y的转化率,但X的转化率要小于乙中X的转化率;同理分析甲和丙,相当于在甲的基础上再增加Y的物质的量,丙中X的转化率大于甲中X的转化率,但Y的转化率要小于甲中Y的转化率;同理分析乙和丁,丁相当于在乙的基础上再增加Y的物质的量,丁中X的转化率大于乙中X的转化率,但Y的转化率要小于乙中Y的转化率;乙和丙比较,相当于在增大压强。由于正方应是体积增大的可逆反应,所以平衡向逆反应方向移动,因此X或Y转化率均降低;故X的转化率甲<丙<乙<丁,同理得Y的转化率:丁<丙<乙<甲,答案(A)。 四、极端法 将研究的对象或过程向极端状态进行分析,使因果关系变得明显,从而使问题得以解决。 例4.在密闭容器中进行X2(g)+4Y2(g) A.c(X2)=0.15 mol·L-1 B.c(Y2)=0.9 mol·L-1 C.c(Z2)=0.3 mol·L-1 D.c(Q2)=0.5mol·L-1 妙法点拨:可逆反应的特点是给定条件下反应进程的限度性,所以反应物和生成物的浓度不可能是0,将反应物X2、Y2按化学计量数全部转化为Z2、Q2,Z2、Q2分别为0.2mol·L-1、0.3mol·L-1,再加上原有的浓度,Z2、Q2的极限浓度是0.4mol·L-1、0.6 mol·L-1,同理将产物Z2、Q2按化学计量数全部转化为X2、Y2,X2、Y2分别为0.1mol·L-1、0.4mol·L-1, 再加上原有的浓度,X2、Y2的极限浓度是分别为0.2mol·L-1、0.8mol·L-1, c(Y2)=0.9 mol/L已超过极限浓度,答案(B)。 五、估算法 由于条件限制,无法(有时也没必要)进行精确地运算和判断, 而只能依赖于估算。 实质上是一种快速的近似计算, 它的基本特点是对数值作适当扩大或缩小,从而对运算结果确定一个范围,或做出一个估计。 例5.将1molCO(g)和1molH2O(g)充入某固定容积的反应器中,在一定条件下CO(g)+ H2O(g) A.22.2% B.28.2% C.33.3% D.37.8% 妙法点拨:因反应前后气体化学计量数没有变化,无论如何进行总物质的量是不变的,由于反应的可逆性和移动性,生成的CO2 最多不能达到1mol,最少不低于2/3,CO2的体积分数介于2/9—1/3之间。答案(B)。 六、差量法 依据化学反应前后气体物质的量之差,与反应物或生成物的变化量成正比而建立的一种解题方法。正确找出“理论差量”,是“差量法”的解题关键。反应前后存在差量,且此差量易求出是使用差量法的前提。 例6.一定条件下,合成氨气反应达到平衡时,测得混合气体中氨气的体积分数为20.0%,与反应前的体积相比,反应后体积缩小的百分率是 A.16.7% B.20.0% C.80.0% D.83.3% 妙法点拨:设达到平衡后混合气体的体积为1L,则其中生成的氨气的体积1L×20.0%=0.2L。根据反应的方程式:  反应后气体体积缩小率 七、三段法 化学平衡计算的一般格式,根据题意和恰当的假设列出起始量、转化量、平衡量。 例7.一定温度下,反应2SO2+O2 A. 0.4mol B. 0.6mol C. 0.8mol D. 1.2mol 妙法点拨:原平衡体系中SO2、O2、SO3的物质的量分别为2a、3a和4a,缩小体积平衡向右移动,O2的转化量为x 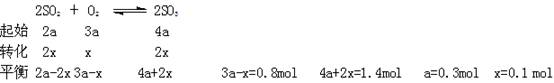 再次达到平衡时,n(SO2)=2×0.3mol-2×0.1mol=0.4mol。答案(A)。 八、整体法 整体法研究化学问题时,暂且避开局部细节或单个因素的纠缠,将需要解决的问题看作一个整体,通过研究问题的整体形式或整体结构作某种整体处理。 例8.如图所示,当关闭K时,向A中充入1mol N2、3mol H2,向B中充入2mol N2、6mol H2,起始时,V(A)=V(B)=aL。在相同温度和催化剂存在的条件下,两容器中各自发生下列反应:N2(g)+3H2(g) 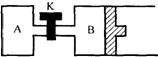 请回答: 打开K,过一段时间重新达平衡(Ⅱ)时,B的体积为 (用含a的代数式表示,连通管中气体体积忽略不计)。 妙法点拨:关闭K时A为恒容,B为恒压,打开K时可容器A、B看作整体,利用B为恒压的处理方式,B中充入2mol N2、6mol H2共8 mol,达到平衡(Ⅰ)时,V(B)=0.8aL , 九、图示法 由题目条件作出符合题意的图形,借助图形的直观性,经过简单推理或计算,从而得到答案的方法。 例9.已知2SO2 (g) + O2 (g) A.容器内压强P:P甲=P丙> 2P乙 B.SO3的质量m:m甲=m丙> 2m乙 C.c(SO2)与c(O2)之比k:k甲=k丙> k乙D.反应放出或吸收热量的数值Q:Q甲=G丙> 2Q乙 妙法点拨: 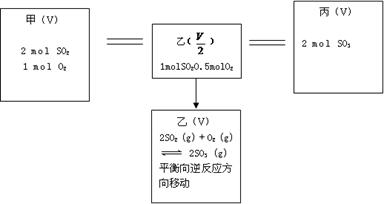 通过体积放缩构建等同平衡,改变体积观察平衡的移动得出结论。A P甲<2P乙,B m甲>2m乙,C K甲=K乙,D Q甲=197-Q丙> 2Q乙。答案(B )。 十、验证法 从题的正面解决困难时,将选项或特值逐一代入题干进行检验,看是否合适。 例10.甲、乙两容器都发生反应 2A(g)+ B(g ) A.若甲、乙两容器均为恒容容器,则 x必等于 2 B.若甲、乙两容器均为恒压容器,则 x必等于 3 C.若甲为恒压容器、乙为恒容容器,且 x≠3,则 n1必大于 n2 D.若甲为恒容容器、乙为恒压容器,且 x= 3,则 n1必大于 n2 妙法点拨:选项中x有两个值2和3,分别代入考虑。恒温恒压下,对x为任何值,两者均为等效平衡,达到平衡时,C的体积分数均相等,B选项错误;x=2甲、乙两容器均为恒容时,平衡混合气中C的体积分数相等,乙容器中充入起始A和B物质的量必须是2 mol、1 mol,0.6 molC转化到左侧,1.4 molA+0.6 molA=2 molA,0.7 molB+0.3molB=1 mol B,x=3反应前后化学计量数相等,压强对反应没有影响,只要投料A、B物质的量之比符合1:2就满足C的体积分数均相等,(1.4 molA+1.2mol/3A):(0.7 molB+0.6 mol/3 molB)=2:1,A选项错误;x≠3,甲、乙两容器一个保持等压、一个保持等容(不考虑温度变化),假设x=2,反应后化学计量数减小,甲和乙投料相同但甲为保持压强不变,相当于乙的加压过程,平衡移动,C的体积分数不可能相同,与题干矛盾;D选项x= 3反应前后化学计量数相等,0.6 molC转化到左侧,相当于1.8molA 、0.9molB,甲乙容器物质的量成正比,n1必大于 n2;答案(D)。 (责任编辑:admin) |
- 上一篇:高考反应热问题解法例谈
- 下一篇:《环境保护》考点透视