《化学物质及其变化》单元检测题二
http://www.newdu.com 2025/12/02 07:12:31 人民教育出版社 佚名 参加讨论
《化学物质及其变化》单元检测题二 贵州省遵义市第二中学 周厚彬 张 健 可能用到的相对原子质量:N 14 O 16 K 39 第一部分 选择题(共60分) 一、选择题(每小题3分,每小题只有1个选项符合题意,20小题,共60分。) 1.符合图中阴影部分的物质是 ( ) A.K2CO3 B.NaCl C. Na2CO3 D.NaHCO3 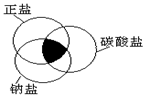 2.2009年11月15日,美国密歇根州大学机械工程系教授约翰哈特为新当选美国总统的奥巴马制造了一组微型头像。他称之为“纳米奥巴马”。每个纳米奥巴马头像包含着1.5亿个碳纳米管。若将碳纳米均匀地分散到蒸馏水中,得到的物质 ( ) ①是溶液 ②是胶体 ③具有丁达尔效应 ④不能透过半透膜 ⑤不能透过滤纸 ⑥静置后会出现黑色沉淀 A.①④⑥ B.②③⑤ C.②③④ D.①③④⑥ 3.厨房中的下列物质,其中属于电解质的是( ) A. CH4 B.铁丝 C. 碳酸钠 D.食盐水 4. 下列家庭小实验不能制得溶液的是( )  5. 日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是( ) A.铜铸塑像上出现铜绿[Cu2(OH)2CO3] B.铁制菜刀生锈 C.大理石雕像被酸雨腐蚀毁坏 D.铝锅表面生成致密的薄膜 6. 加入适量的硝酸银溶液,可使溶液中下列离子数量显著减少的是( ) A. Cl- B. Ba2+ C. NO3- D. Na+ 7. 下列化学方程式不能用离子方程式Ba2++SO42-=BaSO4↓表示的是( ) A. Ba(NO3)2+H2SO4=BaSO4↓+2HNO3 B. BaCl2+Na2SO4=BaSO4↓+2NaCl C. BaCl2+H2SO4=BaSO4↓+2HCl D. BaCO3+H2SO4=BaSO4↓+H2O+CO2↑ 8. 下列离子反应方程式,书写正确的是( ) A. 碳酸钠溶液中加入盐酸 CO32-+2H+=H2O+CO2↑ B. 稀硫酸中加入铁粉 2Fe+6H+=2Fe3++3H2↑ C. 碳酸钙中加入盐酸 CO32-+2H+=H2O+CO2↑ D. 氢氧化钡溶液中加入硫酸 H++OH-=H2O 9. 下列分离、提纯、鉴别物质的方法正确的是( ) A. 用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 B. 用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 C. 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 D. 用加热、蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质 10. 用下图表示的一些物质或概念间的从属关系中不正确的是( )  11.下列溶液的溶质都是电解质,这些溶液中的Cl-浓度与50mL1.5mol/LMgCl2溶液中的Cl-浓度相等的是( ) A.150mL1.5mol/LNaCl溶液 B.75mL0.5mol/LCaCl2溶液 C.150mL2mol/LKCl溶液 D.75mL1mol/LAlCl3溶液 12.用FeCl3溶液腐蚀印刷电路板上铜箔的反应是:2Fe3++Cu === 2Fe2++ Cu2+。下列有关说法错误的是( ) A.Cu是还原剂,被腐蚀 B.Fe3+是氧化剂 C.该反应是置换反应 D.该反应属于离子反应 13.需要加入适当的还原剂才能实现的反应( ) A.PCl3→PCl5 B.MnO4--→Mn2+ C.SO3→HSO3- D.CO2→CaCO3 14. 下列分类标准不正确的是( ) A.分散系分为:溶液、胶体、浊液(标准:分散质粒子的大小) B.化学反应分为:离子反应、非离子反应(标准:是否在水溶液中进行) C.化学反应分为:氧化还原反应、非氧化还原反应(标准:元素化合价是否发生变化) D.化合物分为:电解质、非电解质(标准:溶于水或熔融状态能否导电) 15.在无色透明的未知溶液中加入BaCl2溶液和稀硝酸,产生白色沉淀,则未知溶液中肯定不存在( ) A.Ag+ B.SO42- C.SO32- D.CO32- 16.下列反应中氯元素全部被还原的是( ) A.5Cl2+I2+6H2O=10HCl+2HIO3 B.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O C.MnO2+4HCl=MnCl2+2H2O+Cl2↑ D.2NaCl+2H2O=2NaOH+Cl2↑+H2↑ 17.在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中共存的是 ( ) A.所含溶质为NaHSO4的溶液:加入K+、CO32-、NO3-、Na+ B.滴加酚酞变红的溶液:加入SO42-、Cu2+、K+、Cl- C.含有大量SO42-的溶液:加入K+、Cu2+、Cl-、NO3- D.常温下,加入铁粉能生成H2的溶液:加入Na+、Ca2+、Cl-、HCO3- 18.高铁酸钾(K2FeO4)是一种高效绿色水处理剂,其工业制备的反应原理为: 2Fe(OH)3 + 3KClO + 4KOH = 2K2FeO4 + 3KCl + 5H2O,下列说法正确的是 ( ) A.制高铁酸钾时用KClO作还原剂 B.KCl是还原产物 C.高铁酸钾中铁的化合价为+7价 D.制备高铁酸钾时1mol Fe(OH)3得到6mol 电子 19.已知在酸性溶液中,KMnO4和KI能够反应,具体变化是MnO4-→Mn2+;KI→I2。如果参加反应的KMnO4的物质的量为2mol,则得到的I2最多是 ( ) A.2mol B.5mol C.10mol D.4mol 20.已知R2Ox2-在一定条件下可以与Mn2+反应,使其变为MnO4-,而本身则变为RO42-;又知反应中还原剂与还原产物的物质的量之比为1∶5,则x的值是 ( ) A.7 B.8 C.5 D.4 第二部分 非选择题(共40分) 二、填空题(每空1分,共40分) 21.对物质进行分类是学习化学的重要方法,无机化合物可根据其组成和性质进行分类: 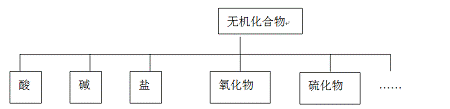 (1)上述所示的物质分类方法名称是 。 (2)以Na、Ca、H、O、C、N中任两种或三种元素组成合适的物质,分别填在下表中②③⑥后面。(各空填写一个化学式即可)
(3)写出⑦转化为⑤的化学方程式: 。 (4)写出①与③反应的离子方程式: 。 (5)写出②与⑥反应的离子方程式: 。 (6)把⑦的气体通⑩的溶液中,产生黄色沉淀,写出反应的化学方程式: 。 22.汽车尾气是城市空气污染来源之一,汽车尾气中含有CO和NO等有害物质。通过特殊的催化装置,可以使CO与NO相互反应生成无害且稳定的气体N2和CO2,反应的化学方程式是: 。 其中氧化剂是 ,还原剂是 ,用双线桥法表示电子的转移 。 23.糕点等食品包装入一个类似干燥剂的小袋——脱氧剂。其作用是吸收氧气,使食物因缺氧而不变质、发霉等,从而长期保存食品。铁脱氧剂就是利用铁易被氧化的性质来吸收氧气,最终产物是Fe2O3?3H2O。有关反应如下: ① 2Fe+O2+2H2O==2Fe(OH)2 ②4Fe(OH)2+O2+2H2O==4Fe(OH)3 ③ 2Fe(OH)3==Fe2O3?3H2O (1)以上反应中,从是否氧化还原反应的角度看,包括 和 两种类型; 从四种基本反应类型的角度看包括 和 两种类型。 (2)反应中作氧化剂的物质有 ,反应中Fe(OH)2是 剂。 24.用一种试剂除去下列物质中的杂质(括号中为杂质),写出所用试剂及离子方程式。 (1)NaNO3溶液(Na2SO4) 除杂试剂: ,离子方程式: 。 (2)FeCl2溶液(FeCl3) 除杂试剂: ,离子方程式: 。 25.火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+C+S===K2S+2NO2↑+CO2↑。其中被还原的元素是 ,被氧化的元素是 (填元素名称),氧化剂是 ,还原剂是 ,氧化产物是 ,还原产物是 ,如果生成4.48L(标况) NO2,转移电子 mol,需要硝酸钾 g。 26.有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、氯化钡溶液、碳酸钾溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各盛少量多次进行两两混合反应,反应现象为:A与B、A与E产生沉淀,B与D、B与E产生沉淀,C与E、D与E产生气体,而C与D无反应现象。由此,可判断各试剂瓶中所盛试剂为 A 、B 、C 、D 、E 另外,请写出下面要求的离子方程式: (1)A与E: 。 (2)B与E: 。 (3)C与E: 。 (4)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式: 。 (5)在以上中性溶液中继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式: 。 《化学物质及其变化》单元检测题 参考答案 一、选择题(每小题3分,每小题只有1个选项符合题意,20小题,共60分。)
二、填空题(每空1分,共40分) 21.(1)树状分类法(2)HNO3;NaOH或Ca(OH) 2;Na2CO3或CaCO3(3)2NaOH+SO2=Na2SO3+H2O (4) H++OH-=H2O(5) CO32-+2H+=H2O+CO2↑或CaCO3+2H+=Ca2++H2O+CO2↑(6)2H2S+SO2=3S↓+2H2O 22. 2CO+ 2NO 催化 N2 + 2CO2 ,NO,CO,略 。 23.(1)氧化还原反应;非氧化还原反应; 化合反应;分解反应。 (2)氧气(O2);还原 24.(1)BaNO3溶液,Ba2++ SO42-= BaSO4 ↓ (2)Fe粉, Fe+2Fe 3+ === 3Fe2+ 25.氮、硫,碳,KNO3、S,C,CO2,K2S、NO2,0.8,20.2。 26. 略 (责任编辑:admin) |