《从实验学化学》单元检测题
http://www.newdu.com 2025/11/13 10:11:05 人民教育出版社 佚名 参加讨论
《从实验学化学》单元检测题 贵州省遵义市第二中学 周厚彬 可能用到的相对原子质量:N:14 H:1 C:12 O:16 S:32 K:39 Cl:35.5 一、选择题(每小题只有一个选项符合题意,每题5分,共60分) 1.在盛放酒精的试剂瓶上应印有如下图所示警示标记中的( )  2.下列化学反应中,属于氧化还原反应的是( ) A.HCl+NaOH=NaCl+H2O B.CaO+ H2O=(OH)2 C.2NaHCO3 3.在某无色透明的酸性溶液中, A.Na+ 、K+、SO42-、HCO3- B.Cu2+、K+、SO42-、NO3- C.Na+、 K+、Cl-、 NO 4.下列说法中正确的是( ) A.1mol氮约含有6.02×1023个粒子 B.1mol H2O中含有1molO原子和2molH原子 C.钠的摩尔质量等于它的相对原子质量 D.硫酸的摩尔质量等于98g 5.世界是由丰富多彩的物质组成,那下列物质中既是金属氧化物又是两性氧化物的是( ) A.Na2O B.CO2 C.Al2O3 D.H2O 6.根据中央电视台报道,近年来,我国的一些沿江或沿海城市多次出现大雾天气,致使高速公路关闭,航班停飞,“雾”属于下列分散系中的( ) A.溶液 B.悬浊液 C.乳浊液 D.胶体 7.“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化及军事科学中。所谓“纳米材料”是指研究、开发出的直径从几纳米至几十纳米的材料,如将纳米材料分散到分散剂中,所得混合物一定具有的性质是( ) A.无色透明 B.有丁达尔效应 C.所得液体呈胶状 D.所得物质一定是悬浊液 8.标准状况下,下列物质占体积最大的是( ) A.98g H2SO4 B.6.02×1023个CO2 C.44.8L HCl D.6g H2w w w .x k 9.下列离子方程式中正 A.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ B.向氢氧化钡溶液中加硫酸溶液:SO42-+Ba2+= BaSO4 C.向稀硫酸溶液中加铁:2Fe + 6 D.向硝酸银溶液中加盐酸:Ag+ + Cl- = AgCl↓ 10. 设NA表示阿伏加德罗常数,下列说法不正确的 A.1 mol醋酸的质量与NA个醋酸分子的质量相等 B.NA个氧气分子和NA个氢气分子的质量比等于16∶1 C.30 g乙烷(C2H6)所含的原子数目为NA D.在标准状况下, 0.5NA个氯气分子所占体积约是11.2 L 11.用FeCl3溶液腐蚀印刷电路板上铜箔的反应是2Fe3++Cu === 2Fe2++ Cu2+。下列有关说法错误的是( ) A.Cu是还原剂 B。Fe3+是氧化剂 C.该反应是置换反应 D。该反应属于离子反应 12.根据反应①2FeCl3+2KI===2FeCl2+2KCl+I2,②2FeCl2+Cl2=2FeCl3,判断下列物质的氧化性由强到弱的顺序中,正确的是( ) A.Fe3+>Cl2>I2 B.Cl2>I2>Fe3+ C.I2>Cl2>Fe3+ D.Cl2>Fe3+>I2 二.填空题:(每空1分,共18分) 13.现有以下物质:①KCl(熔融) ②液态HCl ③稀盐酸 ④Ag ⑤CaCO3固体⑥稀硫酸 ⑦酒精(C2H5OH) ⑧KNO3,⑨液态SO3 ⑩KNO3溶液 ?蔗糖溶液,请回答下列问题(用序号): (1)以上物质中能导电的是_________________。 (2)以上物质中属 (3)以上物质中属于非电解质的是___________。 14.下列三组物质中,均有一种物质的类别与其它三种不同 A.MgO、Na2O、CO2、CuO B.HCl、H2O、H2SO4、HNO3 C (1)三种物质依次是(填化学式):A ;B ;C 。 (2)这三种物质相互作用可生成一种新物质,该反应 氧化还原反应(填“是 (3)写出这种新物质与盐酸反应的离子方程式: 。 (4)写出大理石与稀盐酸反应的离子方程式: 。 (5)写出NaHSO4固体溶于水的电离方程式是: 。 (6)写出石灰乳与稀盐酸反应的离子方程式是: 。 (7)用双线桥法表示下列氧化还原反应,并指出氧化剂。MnO2 + 4HCl(浓) = MnCl2 + 2H2O + Cl2↑氧化剂 。 15.在反应KClO3+6HCl=KCl+3H2O+3Cl2↑中,还原剂是 ,氧化产物是 ,HCl表现出 性和 性;若有3 mol HCl参加反应,则上述反应中转移的电子数为 mol;若反应生成标准状况下的Cl2体积为33.6 L,则需消耗KClO3的质量为 。 三、实验题(每空2分,共16分) 16.掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。 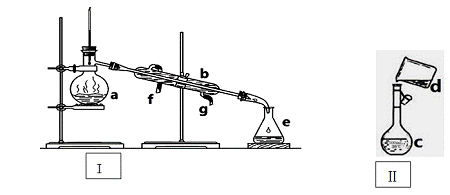 (1)写出下列仪器的名称: a. c. (2)仪器a~e中,使用前必须检查是否漏水的有 。(填序号) (3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是 。 (4)现需配制0.1mol·L-1NaOH溶液450mL,装置II是某同学转移溶液的示意图。 ①图中的错误是 。(写一条) ②配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) 。 A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶 B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解X|k |b| 1 . c|o |m C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中 D.将容量瓶盖紧,振荡,摇匀 E.改用胶头滴管加水,使溶液凹面恰好与刻度相切 F.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处 ③配制0.1 mol· L-1NaOH溶液的实验中,如果出现以下操作: A.称量时用了生锈的砝码 B.将NaOH放在纸张上称量 C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中 D.往容量瓶转移时,有少量液体溅出 E.未洗涤溶解NaOH的烧杯 F.定容时仰视刻度线 G.容量瓶未干燥即用来配制溶液 H.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线 上述操作中对配制的溶液物质的量浓度大小造成(填写字母)偏大的有___________ (5).如果配制的NaOH溶液已经变质含有少量Na2CO3 ,怎样除去?
(6)某学校化学课外活动小组的同学,将一些可溶性化合物溶于水制成甲、乙两种溶液,两种溶液共含有H+、Ag+、K+、Ba2+、OH-、Cl-、NO3-、CO32-8种离子,两种溶液里所含离子各不相同;已知向甲溶液滴入石蕊试液,石蕊试液变成蓝色,则乙溶液里含有的四种离子应该是(填离子符号)______________________________________。 (责任编辑:admin) |